Papillomavirus низкого и высокого канцерогенного риска (6, 11, 44, 16, 18, 26, 31, 33, 35, 39, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82), ДНК генотипирование [реал-тайм ПЦР]
Молекулярно-генетическое исследование, которое позволяет определить и дифференцировать 21 генотип вируса папилломы человека в исследуемом материале, что дает возможность охарактеризовать онкогенный потенциал инфекции и спланировать тактику лечения.
Синонимы русские
Вирус папилломы человека (ВПЧ) с определением генотипа.
Синонимы английские
Human Papillomavirus (HPV), DNA, Genotyping.
Метод исследования
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Мазок из зева (ротоглотки), мазок урогенитальный, мазок урогенитальный (с секретом простаты), ректальный мазок.
Как правильно подготовиться к исследованию?
Подготовки не требуется.
Общая информация об исследовании
Вирус папилломы человека – ДНК-содержащий вирус из семейства паповавирусов, ассоциированный с развитием остроконечных кондилом, бородавок, предраковых изменений аногенитальной области, рака шейки матки. Существует более 100 типов ВГЧ, около 30 из них могут инфицировать половые пути, и около 14 генотипов связаны с развитием рака шейки матки, прямой кишки, полового члена и новообразований других локализаций (например, орофарингеальной плоскоклеточной карциномы).
Онкогенные папиллома-вирусы имеют в составе ДНК белки Е6/Е7, которые способны супрессировать процессы апоптоза (запрограммированной гибели) в клетках с измененным генетическим материалом. Генотипы 1, 2, 3, 5 считаются неонкогенными, а генотипы 6, 11, 42, 43, 44 относятся к папиллома-вирусам низкого онкогенного риска. ВПЧ высокого онкогенного риска – это генотипы 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 и 68.
Основной путь распространения вируса – половой. Возможна вертикальная (от матери к ребенку) и контактно-бытовая передача инфекции. В организм человека может попасть несколько типов ВПЧ одновременно. Заражаются обычно после начала половой жизни в возрасте 16-25 лет. При инфицировании онкогенными генотипами вируса между 25 и 35 годами вероятны интраэпителиальные поражения и через несколько лет развитие рака. В 70 % случаев в течение первого года и в 90 % случаев через 2 года после инфицирования возможно самоизлечение.
Возможна вертикальная (от матери к ребенку) и контактно-бытовая передача инфекции. В организм человека может попасть несколько типов ВПЧ одновременно. Заражаются обычно после начала половой жизни в возрасте 16-25 лет. При инфицировании онкогенными генотипами вируса между 25 и 35 годами вероятны интраэпителиальные поражения и через несколько лет развитие рака. В 70 % случаев в течение первого года и в 90 % случаев через 2 года после инфицирования возможно самоизлечение.
Инфицирование различными путями, а также разными типами вируса обуславливает особенности течения заболевания, локализацию эпителиальных изменений и риск развития неопластических процессов в местах поражения кожи и слизистых. Подошвенные бородавки вызываются генотипами 1, 2, 4, 63, а обычные бородавки – 2-м и 7-м типом ВПЧ. Папиллома-вирус 6-го, 7-го, 11-го, 16-го и 32-го типов может стать причиной папиллом ротовой полости и гортани, а ВПЧ 6-го, 11-го, 42-го, 44-го типов – аногенитальных бородавок. Папилломы, вызванные даже неонкогенными или низкоонкогенными папиллома-вирусами, рекомендовано удалять.
Инфицирование онкогенными вирусами не означает, что у пациента будет раковое заболевание, однако требует дальнейшего тщательного регулярного наблюдения за инфицированным. При выявлении изменений кожи и слизистой с образованием кондилом, бородавок или внутриэпителиальной дисплазии рекомендовано исключение папиллома-вирусной инфекции и определение генотипа вируса, что позволяет оценить риск развития рака и определить тактику лечения.
Полимеразная цепная реакция (ПЦР) выявляет ДНК вируса папилломы человека (ВПЧ) с высокой специфичностью и чувствительностью. Определение ДНК различных генотипов вируса должно обязательно проводиться с учетом результатов цитологического и гистологического исследований биоптата, удаленной папилломы, бородавки, мазка из шейки матки или участка с дисплазией, метаплазией или признаками малигнизации.
Для чего используется исследование?
- Для подтверждения наличия папиллома-вирусной инфекции.

- Для диагностики одновременного инфицирования несколькими типами ВПЧ.
- Для дифференциальной диагностики генотипов ВПЧ.
- Для того чтобы оценить риск развития новообразований, ассоциированных с ВПЧ (рак шейки матки, рак прямой кишки, рак аногенитальной области, орофарингеальная карцинома).
Когда назначается исследование?
- При выявлении цитологических изменений в мазке на атипию, в мазке по Папаниколау.
- При наличии кондилом, бородавок и других морфологических изменений эпителия различных локализаций.
- При выявлении вируса папилломы человека неуточненного типа (по данным лабораторного анализа).
Что означают результаты?
Референсные значения: отрицательно.
Причины положительного результата
- Инфицирование вирусом папилломы человека
- Генотипы низкого онкогенного риска: 6, 11, 44
- ВПЧ высокого онкогенного риска: 16, 18, 26, 31, 33, 35, 39, 45, 51, 52, 53, 56, 58, 59, 66, 73, 68 и 82
Причины отрицательного результата
- Отсутствие генетического материала вируса папилломы человека в исследуемом материале
- Низкое содержание вируса в материале
Что может влиять на результат?
- Ложноотрицательный результат может быть получен при неправильном взятии и хранении материала, а также при содержании вируса в материале ниже детектируемого уровня.

- Ложноположительный результат возможен при загрязнении материала.
Важные замечания
- Инфицирование онкогенными типами ВПЧ не всегда приводит к раку.
- Вероятно одновременное заражение несколькими генотипами ВПЧ.
- Результат анализа должен интерпретироваться с учетом заключений цитологического и гистологического исследований.
Также рекомендуется
- Human Papillomavirus 16/18 (HPV 16/18), ДНК [реал-тайм ПЦР]
- Human Papillomavirus 6/11 (HPV 6/11), ДНК [реал-тайм ПЦР]
- Human Papillomavirus высокого канцерогенного риска (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 типы), ДНК без определения типа [ПЦР]
- Human Papillomavirus высокого канцерогенного риска (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 типы), ДНК генотипирование [реал-тайм ПЦР]
- Human Papillomavirus, ДНК количественно [реал-тайм ПЦР]
- Цитологическое исследование мазков (соскобов) с поверхности шейки матки (наружного маточного зева) и цервикального канала на атипию (три точки)
- Антиген плоскоклеточной карциномы (SCCA)
Кто назначает исследование?
Гинеколог, уролог, проктолог, онколог, дерматовенеролог, оториноларинголог.
Литература
- Arbyn M. et al. (2010). «European Guidelines for Quality Assurance in Cervical Cancer Screening. Second Edition–Summary Document». Annals of Oncology 21 (3): 448–458.
- Saslow D, Solomon D, Lawson HW, et al. American Cancer Society, American Society for Colposcopy and Cervical Pathology, and American Society for Clinical Pathology Screening Guidelines for the Prevention and Early Detection of Cervical Cancer. Am J Clin Pathol. 2012;137:516-542.
- «Genital HPV Infection – CDC Fact Sheet». Centers for Disease Control and Prevention (CDC). April 10, 2008. Retrieved 13 November 2009.
- Chaturvedi, Anil; Maura L. Gillison (March 4, 2010).»Human Papillomavirus and Head and Neck Cancer». In Andrew F. Olshan. Epidemiology, Pathogenesis, and Prevention of Head and Neck Cancer (1st ed.). New York: Springer.
Что такое ДНК и из чего состоит геном человека?
Генетика — сложная наука, но информация и рассуждения о генах и наследственности окружают нас со всех сторон.
 Причем звучат они не только от специалистов. Друзья делают генетические тесты, родственники говорят, что у вас могут быть наследственные проблемы со здоровьем, и многое другое.
Причем звучат они не только от специалистов. Друзья делают генетические тесты, родственники говорят, что у вас могут быть наследственные проблемы со здоровьем, и многое другое.В этой статье расскажем, как обстоят дела на самом деле.
Содержание
- Что такое геном
- Хромосомы и ДНК
- Нуклеотиды и гены
- Что «записано» в генах и как их прочитать?
- Что такое «мусорная ДНК»
- Чем геном отличается от генотипа
- Чем геномика отличается от генетики
- Что показывают генетические тесты
- Проект «Геном человека»
Что такое геном
Геном — это совокупность всего генетического материала, который находится в клетке человеческого организма и определяет его характеристики.
Каждый геном уникален. Именно он определяет, как будет развиваться тело человека, как он будет расти, какая у него будет внешность и как она будет меняться с возрастом.
В геноме также заложено то, как будут работать клетки, ткани и органы тела.
Разберем, из чего состоит геном и как он «хранится» в клетках.
Хромосомы и ДНК
Почти во всех клетках нашего тела есть ядра. Их можно сравнить с «командным центром», который дает клеткам указания расти, делиться или умирать.
Именно в ядре находятся хромосомы. Это структуры, в которых сосредоточена большая часть генетической информации. Каждая хромосома представляет собой одну плотно «упакованную» длинную нить ДНК.
В каждой нормальной клетке человека 23 пары хромосом, то есть всего их 46.
Исключение составляют «родительские» клетки — сперматозоид и яйцеклетка. В каждой из них находится половинный набор хромосом, то есть 23.
ДНК (дезоксирибонуклеиновая кислота) — это длинная молекула, которую принято называть «двойной спиралью». Она хранит биологическую информацию, которая «записана» в виде генетического кода.
ДНК — это длинная нить, построенная из нуклеотидов. Гены — отрезки этой нити.
Нуклеотиды и гены
Информация в ДНК записана в виде кода, состоящего из четырех азотистых оснований:
- аденин (А),
- гуанин (Г),
- цитозин (Ц),
- тимин (Т).
Основания одной цепи соединяются с основаниями другой цепи парами (аденин с тимином, цитозин с гуанином). Каждое основание присоединяется к молекуле сахара и молекуле фосфата — вся эта конструкция называется
Посмотрите еще раз на двойную спираль ДНК: ее горизонтальные «ступени» — это и есть пары оснований, а вертикальные боковые части — сахара и фосфаты.
Теперь, когда мы поняли, как устроена двойная цепочка ДНК, настало время поговорить о генах.
Ген — это основная «единица» наследственной информации, и он представляет собой «кусочек» ДНК, то есть некоторое количество нуклеотидов.
Что «записано» в генах и как их прочитать?
У каждого человека есть две копии большинства генов — по одной от отца и от матери.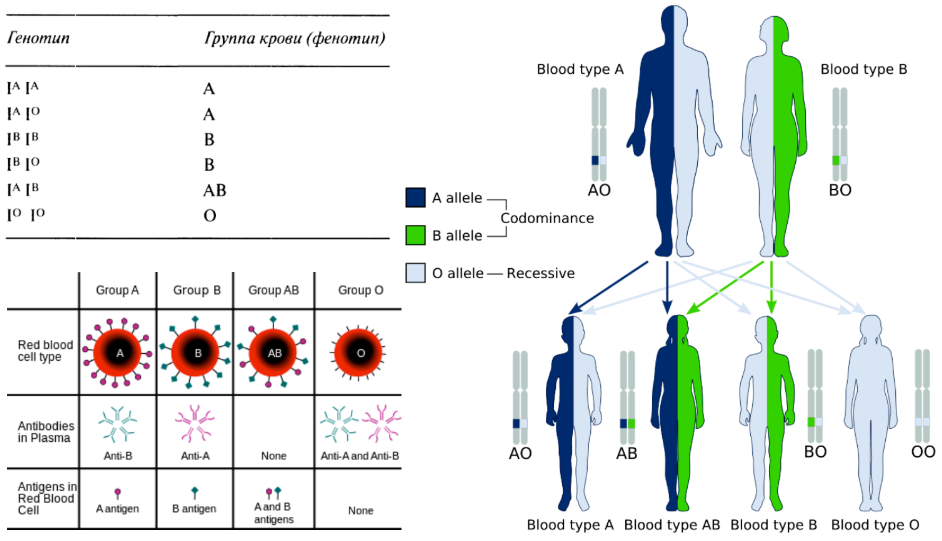 Большинство генов одинаковы для всех людей, но малая часть (около 1%) немного отличаются от человека к человеку.
Большинство генов одинаковы для всех людей, но малая часть (около 1%) немного отличаются от человека к человеку.
Именно этот 1% генов отвечает за уникальные физические особенности каждого из нас.Photo by Ricardo Gomez Angel / Unsplash
Каждый человек обладает 20—25 тысячами генов.
В части генов в виде кода записаны «рецепты» изготовления белков. Именно белки выполняют основные функции для поддержания жизнедеятельности организма: они отвечают за пищеварение, кровообращение, иммунитет, передачу информации между клетками.
Чтобы изготовить белки по записанному в генах коду, специальные соединения, ферменты, «читают» и копируют этот код. В результате получаются длинные одноцепочечные молекулы — РНК (рибонуклеиновые кислоты), но это еще не белок.
РНК лишь несут в себе информацию о первичной структуре белка, поэтому их называют матричными (сокращенно — мРНК). Эти молекулы покидают ядро клетки и перемещаются в ее цитоплазму. Там специальные органы — рибосомы — считывают код мРНК и изготавливают по этому «рецепту» белок.
Там специальные органы — рибосомы — считывают код мРНК и изготавливают по этому «рецепту» белок.
Что такое «мусорная ДНК»
Лишь около 1% ДНК составляют гены, которые кодируют белки.
Считается, что остальные 98—99% ДНК не несут в себе подобной информации. Поэтому долгое время эту часть ДНК считали бесполезной — отсюда и ее название, «мусорная ДНК».
Однако сейчас известно, что на самом деле она выполняет ряд важных функций. В частности, может «включать» и «выключать» гены, регулируя их активность и, как следствие, выработку белков.
Photo by Zonduurzaam Deventer / UnsplashНекоторые участки некодирующей ДНК необходимы для нормального процесса синтеза белков. Кроме того, она служит для защиты хромосом — специальные сегменты некодирующей ДНК (теломеры) «закрывают» концы хромосом и предохраняют от разрушения при делении клетки.
Чем геном отличается от генотипа
И геном, и генотип — это совокупность генов организма. Изначально отличие заключалось в масштабе.
Изначально отличие заключалось в масштабе.
Генотип — это совокупность генов одного человека. От генотипа зависят внешние черты — рост, цвет кожи, глаз, тип волос и так далее. Внешние признаки, закодированные в генотипе, называются фенотипом.
Геном — это совокупность всей генетической информации отдельного человека, включая некодирующую и митохондриальную ДНК. Так как отличия между геномами представителей одного и того же вида незначительны, можно также сказать, что
генотип характеризует одну особь, а геном — вид.
Чем геномика отличается от генетики
Изучением ДНК, нуклеотидов и в целом работы генов занимаются геномика и генетика.
Генетика — это наука, которая изучает гены и их вариации, а также процессы наследования генов и изменчивость признаков человека.
Другими словами, генетики изучают, как определенные черты и свойства организма (в том числе и наследственные заболевания) передаются из поколения в поколение, а также как работа разных генов влияет на организм.
Геномика — это более новый термин. Геномика исследует геном, то есть всю совокупность генов организма, в том числе их взаимодействие как друг с другом, так и с окружающей средой.
Геномика включает в себя и изучение заболеваний, но не сугубо генетических, а мультифакторных, — таких, которые вызываются комбинацией генетических факторов и факторов окружающей среды, например, болезней сердца, астмы, диабета, рака.
Геномика предлагает новые возможности терапии и лечения некоторых сложных заболеваний, а также новые методы диагностики.
Что показывают генетические тесты
Сегодня исследовать свою ДНК очень просто — для этого нужно всего лишь сдать кровь или слюну на генетическое исследование. Но генетические тесты бывают разные.
- Стандартное диагностическое тестирование — используется для подтверждения или исключения определенного генетического заболевания.
- Тест на наличие наследственных заболеваний — проводят до или во время беременности, чтобы определить риск их появления у ребенка.

- Генетический скрининг новорожденных — стандартная процедура, которая проводится для выявления ряда наследственных заболеваний.
- Прогностическое генетическое тестирование — позволяет оценить предрасположенность к развитию ряда заболеваний (например, рака молочной железы) в более позднем возрасте.
- фармакогенетическое тестирование — показывает, может ли генетика человека влиять на его реакцию на лекарства.
Но и это лишь часть возможностей. Так, с помощью генетического теста можно получить более разнообразную информацию.
Генетический тест Атлас позволяет не только узнать о рисках развития ряда заболеваний, но и, например, получить информацию предрасположенности к непереносимости продуктов, вероятности получения спортивных травм. Кроме того, с помощью теста можно узнать о других генетически обусловленных особенностях организма, выяснить, к каким популяциям относились ваши предки и даже найти дальних родственников.
Проект «Геном человека»
Проект«Геном человека» — самый масштабный международный проект по изучению человеческого генома.
Он стартовал в 1990 году и формально был завершен в 2003 году. Фактически цели проекта были выполнены только в 2022 году.
Главная цель проекта — полная расшифровка человеческого генома — определение последовательности пар оснований, которые составляют ДНК, а также выявление всех генов и определение их функций.
К 2003 году ученые смогли «прочитать» 92% «букв» в ДНК. Тогда пробелы не считались важными. Оставшиеся 151 миллион пар оснований (примерно 8% генома) относились к «мусорной» ДНК.
Photo by vnwayne fan / UnsplashОднако за прошедшие годы ученые, используя новейшие технологии, смогли прочитать геном до конца. Оказалось, что остававшиеся непрочитанными 8% генома несут в себе важную информацию, благодаря которой исследователи смогут по-новому интерпретировать полученные ранее данные.
Статьи о генетике в блоге Атласа:
- Что такое эпигенетика
- Генная терапия
- Кто такой врач-генетик и чем он может помочь
- Very Well Health, What Are Genes, DNA, and Chromosomes? 2022
- Your Genome, What is a genome? 2017
- Medline Plus, What is DNA? 2021
- National Human Genome Research Institute, Genome
- National Human Genome Research Institute, Human Genome Project
Обнаружение генотипов, лежащих в основе фенотипов человека: прошлые успехи в лечении менделевской болезни, будущие подходы к комплексным заболеваниям
Ботштейн, Д. , Уайт, Р.Л., Сколник, М. и Дэвис, Р.В. Построение карты генетического сцепления у человека с использованием длины фрагмента рестрикции полиморфизмы. утра. Дж. Хам. Жене. 32 , 314–331 (1980).
, Уайт, Р.Л., Сколник, М. и Дэвис, Р.В. Построение карты генетического сцепления у человека с использованием длины фрагмента рестрикции полиморфизмы. утра. Дж. Хам. Жене. 32 , 314–331 (1980).
КАС пабмед ПабМед Центральный Google Scholar
Федер, Дж.Н. и другие. Новый ген, подобный MHC класса I, мутирует у пациентов с наследственным гемохроматозом. Нац. Жене. 13 , 399–408 (1996).
КАС пабмед Google Scholar
Дрейер, С.Д. и другие. Мутации в LMX1B вызывают аномальное формирование скелета и почечную дисплазию при синдроме ногтевого надколенника. Нац. Жене. 19 , 47–50 (1998).
КАС пабмед Google Scholar
Энаттах, Н.С. и другие. Выявление варианта, связанного с гиполактазией взрослого типа. Нац. Жене. 30 , 233–237 (2002).
Нац. Жене. 30 , 233–237 (2002).
КАС пабмед Google Scholar
Ройер-Покора, Б. и др. Клонирование гена наследственного заболевания человека — хронической гранулематозной болезни — на основе его хромосомной локализации. Природа 322 , 32–38 (1986).
КАС пабмед Google Scholar
Кениг, М. и др. Полное клонирование мышечной дистрофии Дюшенна (МДД). кДНК и предварительная геномная организация гена МДД у нормальных и больных людей. Cell 50 , 509–517 (1987).
КАС пабмед Google Scholar
Керем, Б. и др. Идентификация гена муковисцидоза: генетический анализ. Наука 245 , 1073–1080 (1989).
КАС пабмед Google Scholar
Риордан, Дж. Р. и др. Идентификация гена муковисцидоза: клонирование и характеристика комплементарной ДНК. Наука 245 , 1066–1073 (1989).
Р. и др. Идентификация гена муковисцидоза: клонирование и характеристика комплементарной ДНК. Наука 245 , 1066–1073 (1989).
КАС пабмед Google Scholar
Strathdee, CA, Gavish, H., Shannon, WR & Buchwald, M. Клонирование кДНК для анемии Фанкони путем функциональной комплементации. Природа 356 , 763–767 (1992).
КАС пабмед Google Scholar
Савицкий К. и др. Единственный ген атаксии-телеангиэктазии с продуктом, подобным киназы PI-3. Наука 268 , 1749–1753 (1995).
КАС пабмед Google Scholar
Уоллес, М. Р. и др. Ген нейрофиброматоза типа 1: идентификация большого транскрипта, нарушенного у трех пациентов с NF1. Наука 249 , 181–186 (1990).
КАС пабмед Google Scholar
Фунг Ю. -К.Т. и другие. Структурные доказательства подлинности гена ретинобластомы человека. Наука 236 , 1657–1661 (1987).
-К.Т. и другие. Структурные доказательства подлинности гена ретинобластомы человека. Наука 236 , 1657–1661 (1987).
КАС пабмед Google Scholar
Мики Ю. и др. Сильный кандидат на ген 9 предрасположенности к раку молочной железы и яичников.0004 BRCA1 . Наука 266 , 66–71 (1994).
КАС пабмед Google Scholar
Wooster, R. et al. Идентификация гена предрасположенности к раку молочной железы BRCA2 . Природа 378 , 789–792 (1995).
КАС пабмед Google Scholar
Нишишо И. и др. Мутации генов хромосомы 5q21 у больных САП и колоректальным раком. Наука 253 , 665–669 (1991).
КАС пабмед Google Scholar
Гузелла, Дж. Ф. и др. Полиморфный маркер ДНК, генетически связанный с болезнью Гентингтона. Природа 306 , 234–238 (1983).
Ф. и др. Полиморфный маркер ДНК, генетически связанный с болезнью Гентингтона. Природа 306 , 234–238 (1983).
КАС пабмед Google Scholar
Совместная исследовательская группа по болезни Гентингтона. Новый ген, содержащий тринуклеотидный повтор, который размножается и нестабилен на хромосомах болезни Гентингтона. Cell 72 , 971–983 (1993).
Weber, J.L. & May, P.E. Обширный класс полиморфизмов ДНК человека, которые можно типировать с помощью полимеразной цепной реакции. утра. Дж. Хам. Жене. 44 , 388–396 (1989).
КАС пабмед ПабМед Центральный Google Scholar
Литт, М. и Люти, Дж.А. Гипервариабельный микросателлит, обнаруженный in vitro амплификации динуклеотидного повтора в гене актина сердечной мышцы. утра. Дж. Хам. Жене. 44 , 397–401 (1989).
Дж. Хам. Жене. 44 , 397–401 (1989).
КАС пабмед ПабМед Центральный Google Scholar
Venter, J.C. et al. Последовательность генома человека. Наука 291 , 1304–1351 (2001).
КАС пабмед Google Scholar
Sachidanandam, R. et al. Карта вариаций последовательности генома человека, содержащая 1,42 миллиона однонуклеотидных полиморфизмов. Природа 409 , 928–933 (2001).
КАС пабмед Google Scholar
Ландер Э.С. и Ботштейн, Д. Стратегии изучения гетерогенных генетических признаков у людей с использованием карты сцепления полиморфизмов длины рестрикционных фрагментов. Проц. Натл. акад. науч. США 83 , 7353–7357 (1986).
КАС пабмед ПабМед Центральный Google Scholar
Hall, J. M. et al. Связь семейного рака молочной железы с ранним началом с хромосомой 17q21. Наука 250 , 1684–1689 (1990).
M. et al. Связь семейного рака молочной железы с ранним началом с хромосомой 17q21. Наука 250 , 1684–1689 (1990).
КАС пабмед Google Scholar
Ландер, Э.С. и Ботштейн, Д. Картирование гомозиготности — способ сопоставления рецессивных признаков человека с ДНК инбредных детей. Наука 236 , 1567–1570 (1987).
КАС пабмед Google Scholar
Гшвенд, М. и др. Локус анемии Фанкони на 16q определяется путем картирования гомозиготности. утра. Дж. Хам. Жене. 59 , 377–384 (1996).
КАС пабмед ПабМед Центральный Google Scholar
Саар, К. и др. Локализация гена анемии Фанкони на хромосоме 9p. евро. Дж. Хам. Жене. 6 , 501–508 (1998).
КАС пабмед Google Scholar
Waisfisz, Q. et al. Ген группы Е анемии Фанкони, FANCE , картируется на хромосоме 6p. утра. Дж. Хам. Жене. 64 , 14:00–14:05 (1999).
et al. Ген группы Е анемии Фанкони, FANCE , картируется на хромосоме 6p. утра. Дж. Хам. Жене. 64 , 14:00–14:05 (1999).
КАС пабмед ПабМед Центральный Google Scholar
Болино, А. и др. Локализация гена, ответственного за аутосомно-рецессивную демиелинизирующую невропатию с фокально складчатыми миелиновыми оболочками, на хромосоме 11q23 путем картирования гомозиготности и совместного использования гаплотипов. Гул. Мол. Жене. 5 , 1051–1054 (1996).
КАС пабмед Google Scholar
LeGuern, E. et al. Картирование гомозиготности аутосомно-рецессивной формы демиелинизирующей болезни Шарко-Мари-Тута на хромосому 5q23-q33. Гул. Мол. Жене. 5 , 1685–1688 (1996).
КАС пабмед Google Scholar
Бууш, А. и др. Локус аксональной формы аутосомно-рецессивной болезни Шарко-Мари-Тута картируется на хромосоме 1q21.2q21.3 утра. Дж. Хам. Жене. 65 , 722–727 (1999).
и др. Локус аксональной формы аутосомно-рецессивной болезни Шарко-Мари-Тута картируется на хромосоме 1q21.2q21.3 утра. Дж. Хам. Жене. 65 , 722–727 (1999).
КАС пабмед ПабМед Центральный Google Scholar
Rogers, T. et al. Новый локус аутосомно-рецессивной периферической невропатии в области EGR2 на 10q23. утра. Дж. Хам. Жене. 67 , 664–671 (2000).
КАС пабмед ПабМед Центральный Google Scholar
Леал, А. и др. Второй локус аксональной формы аутосомно-рецессивной болезни Шарко-Мари-Тута картируется на хромосоме 19q13.3. утра. Дж. Хам. Жене. 68 , 269–274 (2001).
КАС пабмед Google Scholar
Лифтон Р.П., Гарави А.Г. и Геллер Д.С. Молекулярные механизмы гипертонии человека. Cell 104 , 545–556 (2001).
Cell 104 , 545–556 (2001).
КАС пабмед Google Scholar
Hastbacka, J. et al. Картирование неравновесия по сцеплению в изолированных популяциях основателей — диастрофическая дисплазия в Финляндии. Нац. Жене. 2 , 204–211 (1992).
КАС пабмед Google Scholar
Озелиус Л.Дж. и др. Сильная аллельная ассоциация между геном торсионной дистонии (DYT1) и локусами на хромосоме 9q34 у евреев-ашкенази. утра. Дж. Хам. Жене. 50 , 619–628 (1992).
КАС пабмед ПабМед Центральный Google Scholar
MacDonald, ME et al. Кандидатная область болезни Гентингтона имеет множество различных гаплотипов. Нац. Жене. 1 , 99–103 (1992).
КАС пабмед Google Scholar
Кляйн, К. и др. Поиск гаплотипа основателя PARK3 в большой когорте пациентов с болезнью Паркинсона из северной Германии. Энн. Гум. Жене. 63 , 285–291 (1999).
и др. Поиск гаплотипа основателя PARK3 в большой когорте пациентов с болезнью Паркинсона из северной Германии. Энн. Гум. Жене. 63 , 285–291 (1999).
КАС пабмед Google Scholar
Сервис, С.К., Ланг, Д.В., Фраймер, Н.Б. и Sandkuijl, L.A. Картирование неравновесного сцепления генов болезней путем реконструкции предковых гаплотипов в популяциях-основателях. утра. Дж. Хам. Жене. 64 , 1728–1738 (1999).
КАС пабмед ПабМед Центральный Google Scholar
Макпик, М.С. и Страс, А. Оценка неравновесия по сцеплению путем распада общих гаплотипов с применением к мелкомасштабному картированию. утра. Дж. Хам. Жене. 65 , 858–875 (1999).
КАС пабмед ПабМед Центральный Google Scholar
Моррис, А. П. и Уиттакер, Дж. К. Мелкомасштабное картирование ассоциаций локусов заболеваний с использованием семейств симплексов. Энн. Гум. Жене. 64 , 223–237 (2000).
П. и Уиттакер, Дж. К. Мелкомасштабное картирование ассоциаций локусов заболеваний с использованием семейств симплексов. Энн. Гум. Жене. 64 , 223–237 (2000).
КАС пабмед Google Scholar
Лам, Дж. К., Родер, К. и Девлин, Б. Точное картирование гаплотипов с помощью эволюционных деревьев. утра. Дж. Хам. Жене. 66 , 659–673 (2000).
КАС пабмед ПабМед Центральный Google Scholar
Лю, Дж.С. и другие. Байесовский анализ гаплотипов для картирования неравновесного сцепления. Рез. генома. 11 , 1716–24 (2001).
КАС пабмед ПабМед Центральный Google Scholar
Браунштейн, Б.Х. и другие. Выделение однокопийных генов человека из библиотеки клонов искусственных хромосом дрожжей. Наука 244 , 1348–1351 (1989).
Наука 244 , 1348–1351 (1989).
КАС пабмед Google Scholar
Кокс, Д.Р. и другие. Радиационное гибридное картирование: генетический метод соматических клеток для построения карт хромосом млекопитающих с высоким разрешением. Наука 250 , 245–250 (1990).
КАС пабмед Google Scholar
Кравчак, М. и др. База данных мутаций генов человека — ресурс биомедицинской информации и исследований. Гул. Мутат. 15 , 45–51 (2000).
КАС пабмед Google Scholar
Grantham, R. Формула различия аминокислот, помогающая объяснить эволюцию белков. Наука 185 , 862–864 (1974).
КАС пабмед Google Scholar
Кравчак М. , Болл Э.В. и Купер, Д.Н. Влияние соседних нуклеотидов на скорость замены одной пары оснований зародышевой линии в генах человека. утра. Дж. Хам. Жене. 63 , 474–488 (1998).
, Болл Э.В. и Купер, Д.Н. Влияние соседних нуклеотидов на скорость замены одной пары оснований зародышевой линии в генах человека. утра. Дж. Хам. Жене. 63 , 474–488 (1998).
КАС пабмед ПабМед Центральный Google Scholar
Стивенс, Дж. К. и др. Изменчивость гаплотипов и неравновесие по сцеплению в 313 генах человека. Наука 293 , 489–493 (2001).
КАС пабмед Google Scholar
Миллер, М.П. и Кумар, С. Понимание мутаций болезней человека с помощью межвидовой генетической изменчивости. Гул. Мол. Жене. 10 , 2319–2328 (2001).
КАС пабмед Google Scholar
Gillard, E.F. et al. Молекулярный и фенотипический анализ пациентов с делециями в богатой делециями области гена мышечной дистрофии Дюшенна (МДД). утра. Дж. Хам. Жене. 45 , 507–520 (1989).
утра. Дж. Хам. Жене. 45 , 507–520 (1989).
КАС пабмед ПабМед Центральный Google Scholar
Мията Т., Миядзава С. и Ясунага Т. Два типа аминокислотных замен в эволюции белков. Дж. Мол. Эвол. 12 , 219–236 (1979).
КАС пабмед Google Scholar
Risch, N. Гемохроматоз, HFE и генетическая сложность. Нац. Жене. 17 , 375–376 (1997).
КАС пабмед Google Scholar
Грабовский Г.А. Болезнь Гоше: частоты генов и корреляции генотип/фенотип. Жен. Тест. 1 , 5–12 (1997).
КАС пабмед Google Scholar
Palzkill, T. & Botstein, D. Исследование структуры и функции β-лактамазы с помощью мутагенеза со случайной заменой. Структура белков. Функц. Жене. 14 , 29–44 (1992).
Структура белков. Функц. Жене. 14 , 29–44 (1992).
КАС пабмед Google Scholar
Риш Н. и Мерикангас К. Будущее генетических исследований сложных заболеваний человека. Наука 273 , 1516–1517 (1996).
КАС пабмед Google Scholar
Ландер Э.С. Новая геномика: глобальные взгляды на биологию. Наука 274 , 536–539 (1996).
КАС пабмед Google Scholar
Риш Н. Поиски генетических детерминант в новом тысячелетии. Природа 405 , 847–856 (2000).
КАС пабмед Google Scholar
Пелтонен, Л. и МакКусик, В.А. Анализ болезней человека в постгеномную эпоху. Наука 291 , 1224–1228 (2001).
КАС пабмед Google Scholar
Март, Г. и др. Однонуклеотидные полиморфизмы в открытом доступе: насколько они полезны? Нац. Жене. 27 , 371–372 (2001).
КАС пабмед Google Scholar
Патил, Н. и др. Блоки ограниченного разнообразия гаплотипов, обнаруженные при сканировании с высоким разрешением хромосомы 21 человека. Science 294 , 1719–1723 (2001).
КАС пабмед Google Scholar
Коллинз, Ф.С., Гайер, М.С. и Чакраварти, А. Вариации на тему: каталогизация вариаций последовательности ДНК человека. Наука 278 , 1580–1581 (1997).
КАС пабмед Google Scholar
Габриэль С.Б. и другие. Структура блоков гаплотипов в геноме человека. Наука 296 , 2225–2229 (2002).
Наука 296 , 2225–2229 (2002).
КАС пабмед Google Scholar
Дейли М.Дж. и др. Структура гаплотипов высокого разрешения в геноме человека. Нац. Жене. 29 , 229–232 (2001).
КАС пабмед Google Scholar
Джеффрис А.Дж., Кауппи Л. и Нойманн Р. Интенсивная точечная мейотическая рекомбинация в области класса II главного комплекса гистосовместимости. Нац. Жене. 29 , 217–222 (2001).
КАС пабмед Google Scholar
Cargill, M. et al. Характеристика однонуклеотидных полиморфизмов в кодирующих областях генов человека. Нац. Жене. 22 , 231–238 (1999).
КАС пабмед Google Scholar
Галушка М. К. и другие. Паттерны однонуклеотидных полиморфизмов в генах-кандидатах гомеостаза артериального давления. Нац. Жене. 22 , 239–247 (1999).
К. и другие. Паттерны однонуклеотидных полиморфизмов в генах-кандидатах гомеостаза артериального давления. Нац. Жене. 22 , 239–247 (1999).
КАС пабмед Google Scholar
Вайс, К.М. и Тервиллигер, Дж. Д. Сколько болезней нужно, чтобы нанести на карту ген с SNP? Нац. Жене. 26 , 151–157 (2000).
КАС пабмед Google Scholar
Райт, А.Ф. и Хасти, Н.Д. Сложные генетические заболевания: полемика по поводу кода Креза. Геном Биол. 2 , КОММЕНТАРИЙ 2007 (2001).
Altmuller, J. et al. Полногеномное сканирование сложных заболеваний человека: трудно найти истинную связь. утра. Дж. Хам. Жене. 69 , 936–950 (2001).
КАС пабмед ПабМед Центральный Google Scholar
Glatt, C. E. et al. Скрининг большой эталонной выборки для выявления очень низкочастотных вариантов последовательностей: сравнение двух генов. Нац. Жене. 27 , 435–438 (2001).
E. et al. Скрининг большой эталонной выборки для выявления очень низкочастотных вариантов последовательностей: сравнение двух генов. Нац. Жене. 27 , 435–438 (2001).
КАС пабмед Google Scholar
Дин, М. и др. Типирование полиморфных примесей в этнических популяциях человека. утра. Дж. Хам. Жене. 55 , 788–808 (1994).
КАС пабмед ПабМед Центральный Google Scholar
Калафель, Ф. и др. Эволюция полиморфизма коротких тандемных повторов у человека. евро. Дж. Хам. Жене. 6 , 38–49 (1998).
КАС пабмед Google Scholar
Осье, М.В. и другие. Глобальная перспектива генетической изменчивости генов ADH выявляет необычные паттерны неравновесия по сцеплению и разнообразия. утра. Дж. Хам. Жене. 71 , 84–99 (2002).
Дж. Хам. Жене. 71 , 84–99 (2002).
КАС пабмед ПабМед Центральный Google Scholar
Мюллер-Мыхсок Б. и Абель Л. Генетический анализ сложных заболеваний. Наука 275 , 1328–1329 (1997).
КАС пабмед Google Scholar
Риш, Н. и Тенг, Дж. Относительная сила семейных планов и планов случай-контроль для исследований неравновесия по сцеплению сложных заболеваний человека I. Объединение ДНК. Рез. генома. 8 , 1273–1288 (1998).
КАС пабмед Google Scholar
Hirschhorn, J.N., Lohmueller, K., Byrne, E. & Hirschhorn, K. Всесторонний обзор исследований генетической ассоциации. Жен. Мед. 4 , 45–61 (2002).
КАС пабмед Google Scholar
Сидоу А. Сначала последовательность, потом вопросы. Cell 111 , 13–16 (2002).
Сначала последовательность, потом вопросы. Cell 111 , 13–16 (2002).
КАС пабмед Google Scholar
Апарисио, С. и др. Полногеномная сборка и анализ генома Fugu rubripes . Наука 297 , 1301–1310 (2002).
КАС пабмед Google Scholar
Генотипирование человека | Микрочипы для изучения населения и болезней
Упрощение генотипирования человека
На сегодняшний день усилия по генотипированию человека выявили тысячи ассоциаций между генетическими вариантами и болезнями или признаками и создали карты уникальных вариаций внутри популяций. Микрочипы — идеальная платформа для оценки известных маркеров в геноме человека, позволяющая исследователям находить однонуклеотидные полиморфизмы (SNP) или более крупные структурные изменения среди миллионов маркеров.
Используя массивы для генотипирования человека Illumina, вы можете выбрать профессионально разработанный контент, использовать маркеры, разработанные консорциумом, или настроить содержимое массива в соответствии с целями вашего исследования. Наши решения для микрочипов обеспечивают надежную производительность и поддерживают высокопроизводительную мультиплексную обработку для крупномасштабных популяционных исследований, клинических исследований и других проектов по генотипированию человека.
Наши решения для микрочипов обеспечивают надежную производительность и поддерживают высокопроизводительную мультиплексную обработку для крупномасштабных популяционных исследований, клинических исследований и других проектов по генотипированию человека.
Преимущества генотипирования человека с помощью массивов
Матрицы для генотипирования человека Illumina обладают рядом преимуществ.
- Надежное качество данных благодаря широко распространенной технологии Infinium
- Высокое разрешение для обнаружения вариаций числа копий (CNV), потери гетерозиготности (LOH) и вставок/делеций
- Охват распространенных и редких вариантов, а также различных глобальных популяций
- Высокопроизводительная обработка мультиплексных массивов
- Низкая стоимость образца
- Интеграция с системами секвенирования Illumina для мультиомного анализа
Избранные исследования генотипирования человека
Оценка полигенного риска может стать полезным инструментом в наборе инструментов врача
Исследователи проводят масштабные исследования GWAS с помощью Global Screening Array для выявления связанных с заболеванием локусов ДНК риска и разработки PRS для клинической проверки.
Индивидуальное генетическое тестирование в Японии и Юго-Восточной Азии
Genesis Healthcare предлагает ряд наборов для здоровья и хорошего самочувствия, предназначенных непосредственно для потребителей, чтобы дать людям возможность активно корректировать свой образ жизни.
Прочитать интервьюСлужба подбора генетических данных для исследователей
Sano Genetics предоставляет исследователям ценную информацию о редких заболеваниях, защищая конфиденциальность отдельных лиц.
Прочитать интервьюРабочий процесс массива генотипирования человека
Выберите из готовых к использованию массивов для генотипирования человека с экспертно разработанным содержимым или создайте собственные iSelect или полузаказные массивы в соответствии с конкретными исследовательскими потребностями. Обрабатывайте и сканируйте массивы с помощью быстрого трехдневного рабочего процесса.*
*Infinium XT предлагает вариант двухдневного рабочего процесса.
Щелкните ниже, чтобы просмотреть продукты для каждого этапа рабочего процесса.
- Выбрать содержимое
- Массивы обработки и сканирования
- Отслеживание, анализ и отчет
Комплексное решение для микрочипов для промышленного генотипирования человека с гибким содержанием.
Селектор набора микрочиповНайдите лучший набор для ваших нужд в зависимости от типа проекта, исходного материала, метода или области применения.
Все наборы микрочиповГотовые к использованию наборы микрочипов для генотипирования человека и эпигенетического анализа.
DesignStudio Microarray Assay DesignerВеб-инструмент для разработки пользовательских матриц.
Система iScanСканер микрочипов для высокопроизводительной обработки тысяч образцов в день.
Наборы аксессуаров Infinium Оборудование, программное обеспечение и аксессуары, необходимые для параллельной обработки нескольких образцов массива.
Возможности роботизированной обработки жидкостей, управляющее программное обеспечение и другие опции для автоматизации рабочего процесса массива и уменьшения количества ошибок.
AutoLoader 2.xЭто устройство автоматически загружает носители массива в системы сканирования.
Array Data Analysis SolutionsПрограммное обеспечение для визуализации, анализа и управления данными генотипирования человека.
BaseSpace Clarity LIMSСистема управления лабораторной информацией для лабораторий, проводящих секвенирование и эксперименты с массивами.
BaseSpace Correlation EngineВеб-инструменты для ранних стадий исследований с целью определения механизмов заболевания, мишеней для лекарств и прогностических или прогностических биомаркеров.
Массив Infinium Global Diversity с расширенным содержимым PGx
Представляем наиболее полный микрочип для генотипирования на рынке для фармакогеномных (PGx) исследований с >1,9 млн. маркеры, доступ к высокоэффективным генам PGx и дополнительное программное обеспечение для составления отчетов с вызовом звездных аллелей и метаболизатором
отчетность о состоянии.
маркеры, доступ к высокоэффективным генам PGx и дополнительное программное обеспечение для составления отчетов с вызовом звездных аллелей и метаболизатором
отчетность о состоянии.
Связанные решения
Мутации зародышевой линии рака
Изучение предрасположенности к раку и риска рака с помощью микрочипов Illumina, систем секвенирования и программного обеспечения для анализа данных. Узнайте больше об анализе мутаций зародышевой линии рака.
Полногеномные ассоциативные исследования (GWAS)
Полногеномные ассоциативные исследования (GWAS) используют высокопроизводительную геномику для быстрого сканирования полных геномов больших групп с целью поиска генетических вариантов, коррелирующих с признаком или заболеванием. Узнайте больше о GWAS.
Дополнительные ресурсы
Полногеномное генотипирование
Полногеномные массивы используют высокоинформативные полногеномные теги SNP, обнаруженные в различных популяциях
для масштабных исследований.
Целевое генотипирование
Выполнение скрининга генотипа больших популяций на предмет целевых SNP, направленных на определенные признаки или интересующие гены.
Узнать большеРуководство по методам
Вся необходимая информация: от чипов BeadChips до подготовки библиотеки, выбора секвенатора и анализа. Выберите лучшие инструменты для своей лаборатории.
Руководство по доступуЭпигенетические изменения, связанные с деменцией
Доктор Джон Милл из Королевского колледжа Лондона использует массивы метилирования для изучения эпигенетических изменений, которые способствуют к нейродегенеративным расстройствам.
Доступ к PDFКонсорциумы по генотипированию
Панели Illumina BeadChip для генотипирования являются основой > 25 продуктов консорциумов.
ПодробнееУслуги микрочипов
Эксперты Illumina предоставляют услуги по метилированию и генотипированию.



