Бытовые аллергены
Комплексное исследование, которое позволяет определить сенсибилизацию к наиболее часто выявляемым в клинической практике бытовым аллергенам. Результат выдается по каждому аллергену, входящему в состав исследования.
Синонимы русские
Специфические иммуноглобулины класса Е к домашней пыли, плесени, домашним животным, птицам, тараканам.
Синонимы английские
ImmunoCAP — household allergens.
Метод исследования
Иммунофлюоресценция на твердой фазе (ImmunoCAP).
Единицы измерения
кЕдА/л (килоединица аллергена на литр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Аллерген – это вещество, вызывающее специфическую реакцию организма, называемую аллергией.
Один из основных путей попадания аллергена в организм – ингаляционный, а наиболее распространенными аллергенами, которые обуславливают круглогодичные симптомы, являются бытовые аллергены.
В ходе данного анализа определяются специфические IgE к наиболее распространенным бытовым аллергенам методом ImmunoCAP. ImmunoCAP характеризуется высокой точностью и специфичностью: в малом количестве крови обнаруживаются даже очень низкие концентрации IgE-антител. Исследование является революционным и основано на иммунофлюоресцентном методе, что позволяет увеличить чувствительность в несколько раз по сравнению с другими анализами.
Таким образом, выявление специфических IgE с помощью данной методики выводит аллергодиагностику на качественно новый уровень.
Домашняя пыль — аллерген Greer — становится частой причиной аллергических реакций, которые проявляются аллергическим ринитом, бронхиальной астмой, атопическим дерматитом. При бытовой сенсибилизации аллергический конъюнктивит наблюдается несколько реже, чем при пыльцевой, что объясняется более крупными размерами частиц бытовых аллергенов. В состав домашней пыли входят клещи домашней пыли и продукты их жизнедеятельности, споры плесневых грибов, выделения домашних животных, аллергены тараканов, бактерии, растительные и неорганические частицы, органические соединения из синтетических напольных покрытий, мебели.
Клещи домашней пыли являются одними из основных источников аллергенов в помещениях и составляют большую часть домашней пыли. Данные членистоногие размером около 0,3 мм не видны невооруженным глазом. Они питаются перхотью человека, которая накапливается в матрасах, подушках, на полу, коврах, мягких игрушках и мягкой мебели. Среди представителей домашних клещей наиболее значимыми для развития аллергических реакций являются Dermatophagoides farinae и Dermatophagoides pteronyssinus. D. pteronyssinus предпочитает более влажную среду, чем D. farinae. Считается, что около 50% пациентов с аллергией и около 80% детей с бронхиальной астмой сенсибилизированы к пылевым клещам.
Микроскопические плесневые грибы являются частой причиной тяжелой бронхиальной астмы, аллергического ринита, аллергического синусита и других респираторных аллергозов. Споры и фрагменты плесневых грибов встречаются повсеместно и могут обуславливать круглогодичные аллергические симптомы. Грибы бывают как наружными, так и внутренними источниками аллергенов. На улице микроскопические грибы активно размножаются в почве, листве. В помещениях споры плесени входят в состав пыли. Местами роста грибов могут служить места хранения продуктов, загрязненная обивка, контейнеры для мусора, другие органические субстраты, обычные обои, длительно сохраняющие сырость синтетические материалы, кондиционеры, цветочные горшки. Кроме того, грибы способны расти и на других поверхностях при наличии нужной влажности. Подвальные или холодные внешние стены, лепные украшения окон, занавески в душевой и крепления – также типичные участки роста грибов. В воздухе концентрация спор грибов увеличивается при проветривании сырых помещений.
Грибы бывают как наружными, так и внутренними источниками аллергенов. На улице микроскопические грибы активно размножаются в почве, листве. В помещениях споры плесени входят в состав пыли. Местами роста грибов могут служить места хранения продуктов, загрязненная обивка, контейнеры для мусора, другие органические субстраты, обычные обои, длительно сохраняющие сырость синтетические материалы, кондиционеры, цветочные горшки. Кроме того, грибы способны расти и на других поверхностях при наличии нужной влажности. Подвальные или холодные внешние стены, лепные украшения окон, занавески в душевой и крепления – также типичные участки роста грибов. В воздухе концентрация спор грибов увеличивается при проветривании сырых помещений.  Penicillium chrysogenum (также известный как P. notatum) выявляется преимущественно в помещениях, в хранилищах продуктов, на складах.
Penicillium chrysogenum (также известный как P. notatum) выявляется преимущественно в помещениях, в хранилищах продуктов, на складах.
Во всем мире существует около 3500 разновидностей тараканов, но только пять видов могут вызывать аллергические реакции. Среди них наиболее частый и распространенный источник внутренних аэроаллергенов — рыжий таракан (прусак), который обитает в жилищах и является практически всеядным насекомым. Его аллергены содержатся в слюне, выделениях, фекалиях, оболочке яиц и в мертвых особях. Наибольшая концентрация аллергенов обычно отмечается в помещении кухни, причем они могут находиться не только в воздухе, но и в загрязненных пищевых продуктах.
Также в ходе анализа определяются специфические IgE к аллергенам перьев птиц — гуся, курицы, утки, индейки. Как правило, аллергическая реакция может развиться не столько на само перо, сколько на остатки белков, которые попадают на перья в процессе жизнедеятельности птицы (слюна, оперение и выделения кожи).
 Поэтому люди, чувствительные к этим аллергенам, могут страдать от аллергии, даже не имея непосредственного контакта с ними, а просто находясь рядом с человеком, периодически контактирующего с аллергенами птиц. В основном аллергию провоцируют белки-антигены, которые содержатся на самих перьях, а также в экскрементах птиц. Также вызывают аллергическую реакцию мелкие клещи, которые паразитируют на коже и перьях птиц. Такой вариант возможен при содержании птицы в домашних условиях или при профессиональном контакте у людей, занимающихся селекцией.
Поэтому люди, чувствительные к этим аллергенам, могут страдать от аллергии, даже не имея непосредственного контакта с ними, а просто находясь рядом с человеком, периодически контактирующего с аллергенами птиц. В основном аллергию провоцируют белки-антигены, которые содержатся на самих перьях, а также в экскрементах птиц. Также вызывают аллергическую реакцию мелкие клещи, которые паразитируют на коже и перьях птиц. Такой вариант возможен при содержании птицы в домашних условиях или при профессиональном контакте у людей, занимающихся селекцией.Сенсибилизация к аллергенам животных может вызывать выраженные аллергические реакции и заболевания. Основным путем попадания аллергена в организм является ингаляционный, с развитием респираторных симптомов аллергии, покраснением и зудом глаз, отеком век, чиханием, ринореей, кашлем, бронхоспазмом, одышкой. При попадании аллергенов на кожу у сенсибилизированнных лиц может возникнуть аллергический дерматит, крапивница. Существует заблуждение, что аллергию вызывает шерсть животных, но это не так.
 Существует перекрестная реактивность между некоторыми аллергенами кошек и собак, а также других животных (например, лошадей, овец, свиней, мышей и крыс), поэтому нередко выявляется гиперчувствительность сразу к нескольким видам животных.
Существует перекрестная реактивность между некоторыми аллергенами кошек и собак, а также других животных (например, лошадей, овец, свиней, мышей и крыс), поэтому нередко выявляется гиперчувствительность сразу к нескольким видам животных.Для чего используется исследование?
- Выявление сенсибилизации к бытовым аллергенам у детей и взрослых;
- определение возможных причин аллергического заболевания (аллергического ринита/риноконъюнктивита, бронхиальной астмы, атопического дерматита) с круглогодичным характером течения;
- решение вопроса о целесообразности определения специфических IgE к отдельным аллергенам данной группы.
Когда назначается исследование?
- При подозрении на круглогодичную аллергию у детей и взрослых;
- при обследовании пациентов с покраснением и жжением глаз, отеком век, слезотечением, чиханием, заложенностью, ринореей, зудом в носу, кашлем, одышкой, бронхоспазмом, аллергическим дерматитом;
- при невозможности проведения кожных проб.

Что означают результаты?
Референсные значения (для каждого аллергена): 0 — 0,35 кЕдА/л.
Причины положительного результата по конкретному аллергену:
- сенсибилизация к данному аллергену;
- обострения аллергического риноконъюнктивита, бронхиальной астмы или атопического дерматита, вероятно, обусловленных сенсибилизацией к аллергену.
Причины отрицательного результата по конкретному аллергену:
- отсутствие сенсибилизации к указанному аллергену;
- длительное ограничение или исключение контакта с аллергенами.
Важные замечания
- Выполнение данного исследования безопасно для пациента по сравнению с кожными тестами (in vivo), так как исключает контакт пациента с аллергеном. Прием антигистаминных препаратов и возрастные особенности не влияют на качество и точность исследования.
Также рекомендуется
- Клинический анализ крови: общий анализ, лейкоцитарная формула, СОЭ (с микроскопией мазка крови при выявлении патологических изменений)
- Суммарные иммуноглобулины E (IgE) в сыворотке
- Аллерген h3 — домашняя пыль (Hollister), IgE (ImmunoCAP)
- Смесь аллергенов животных ex2 (ImmunoCAP), IgE: перхоть кошки, перхоть собаки, эпителий морской свинки, крыса, мышь
+ определение специфических иммуноглобулинов класса E к прочим аллергенам
Кто назначает исследование?
Аллерголог, пульмонолог, оториноларинголог, дерматолог, педиатр, терапевт, врач общей практики.
Литература
- Thomas WR, Smith WA, Hales BJ. The allergenic specificities of the house dust mite. Chang Gung Med J 2004;27(8):563-9.
- Chapman MD, Vailes LD, Hayden ML, Platts-Mills TAE, Arruda LK. Cockroach allergens and their role in asthma. In Kay AB, editor. Allergy and allergic diseases. Oxford, UK: Blackwell Science Ltd; 1996:942-51.
- Berzhets BM, Petrova NS, Barashkina OF, Efremenko II, Dotsenko EA, Prishchepa IM. Role of cockroaches Blatella germanica in the development of atopic bronchial asthma. [Russian] Zh Mikrobiol Epidemiol Immunobiol 2001;(4):43-6.
- Platts-Mills TA, Rakes G, Heymann PW. The relevance of allergen exposure to the development of asthma in childhood. J Allergy Clin Immunol 2000;105(2 Pt 2):S503-8.
Сенсибилизация к пыли (аллергии) — медицинская причина уборки; разбираемся, как лечить / Хабр
Пылевой клещ. Размер колеблется от 0,1 до 0,5 мм
Обычная клиническая картина сенсибилизации к пыли у ребёнка и у взрослого выглядит так: человек заходит домой с улицы, и начинается веселье — чихание, так называемый «аллергический салют» (это когда постоянно теребят кончик носа по причине мучительного зуда). Чихание мучает вплоть до обструкции (сужение бронхов в силу аллергического воспаления, что вызывает свистящее дыхание).
Чихание мучает вплоть до обструкции (сужение бронхов в силу аллергического воспаления, что вызывает свистящее дыхание).
Второе по частоте выглядит так: после ОРВИ прошло уже больше 10 дней, а заложенность носа сохраняется на месяц.
Бытовая пыль — это одна из причин, по которым мы вынуждены регулярно делать уборку. Для кого-то она может стать причиной аллергии. В каждом конкретном доме её состав будет различаться, но основные компоненты этого «салата» одинаковы: пылевые клещи и отходы их жизнедеятельности, шерсть животных, частички эпидермиса, грибки плесени, частички еды. Как правило, аллергию вызывают клещи, шерсть и грибок.
Так что если дома вы начинаете чихать, кашлять и постоянно чешется нос, а на улице все симптомы пропадают — это тревожные звоночки.
Давайте разберёмся, как медицина умеет диагностировать аллергию на пыль сегодня и что мы делаем для того, чтобы облегчить страдания аллергиков.
Про аллергены в пыли
Один из самых серьёзных аллергенов в составе домашней пыли — пылевой клещ. Нравится нам это или нет, но пылевые клещи — наши постоянные сожители. Вообще в природе существует около 150 разных их видов, но в основном сенсибилизация случается к дерматофагиодным клещам с романтичными названиями dermatophagoides farina и dermatophagoides pteronissinus. Возбудителями аллергии являются сам клещ, мелкие его фрагменты и продукты жизнедеятельности (в особенности фекалии). За один день продуктивный клещ формирует 10–20 фекальных шариков, которые могут сохраняться в домашней пыли ещё целых полтора года.
Нравится нам это или нет, но пылевые клещи — наши постоянные сожители. Вообще в природе существует около 150 разных их видов, но в основном сенсибилизация случается к дерматофагиодным клещам с романтичными названиями dermatophagoides farina и dermatophagoides pteronissinus. Возбудителями аллергии являются сам клещ, мелкие его фрагменты и продукты жизнедеятельности (в особенности фекалии). За один день продуктивный клещ формирует 10–20 фекальных шариков, которые могут сохраняться в домашней пыли ещё целых полтора года.
Питаются эти товарищи омертвевшими частичками нашей кожи, которые скапливаются в матрасах и подушках, постельных принадлежностях, коврах, игрушках, мягкой мебели. Такого корма для клещей мы производим ежедневно примерно по 1,5 г с человека.
Пылевые клещи максимально комфортно чувствуют себя во влажных и тёплых условиях (80 % относительной влажности и выше 20 градусов по Цельсию). Если влажность опустится ниже 50 %, то клещи высохнут и погибнут.
С клещами вкратце разобрались, остались грибки, шерсть и эпидермис домашних животных. Откуда берутся последние компоненты — вполне очевидно, а вот грибки, например, живут в земле в горшках наших комнатных растений или на стенах квартиры, в ванной комнате.
Откуда берутся последние компоненты — вполне очевидно, а вот грибки, например, живут в земле в горшках наших комнатных растений или на стенах квартиры, в ванной комнате.
Как диагностировать аллергию?
Зелёным отмечена глоточная миндалина, которая разрастается из-за хронического воспаления.
У ребёнка в отличие от взрослого бывают воспалительные заболевания носоглотки — аденоиды. Этим термином называют увеличенную глоточную миндалину, которая нарушает носовое дыхание и потенциально может перекрыть евстахиевы трубы со стороны носоглотки. Аденоидные вегетации характерны для детского организма (в основном от трёх до семи лет), со взрослыми это случается довольно редко. Связано это со сложным процессом формирования иммунной системы в детском возрасте.
На этом этапе важно понять, что именно терзает наш организм — аллергия или заболевание носоглотки. Чтобы не перепутать аллергическую реакцию, например, с ринитом, необходимо пройти осмотр у ЛОРа с проведением эндоскопии.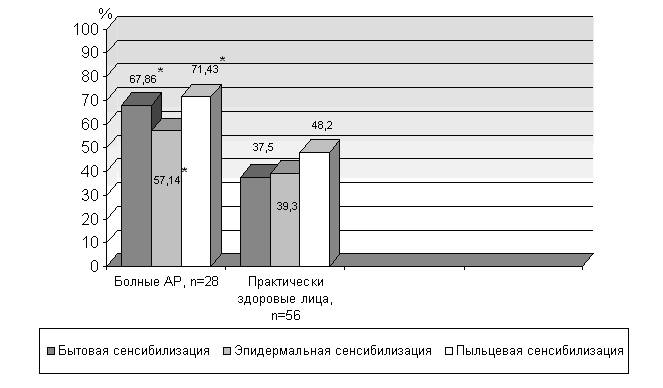 Ротовую полость нужно проверить у стоматолога, чтобы вылечить кариес. В противном случае можно начать лечить аллергию и ничего не вылечить, потому что процессу будут мешать хронические заболевания носоглотки. Поэтому к диагностике мы подходим очень ответственно, и здесь я не обойдусь без клише: в каждом случае всё индивидуально. Волшебных таблеток, которые можно было бы выпить всем подряд и сразу стало бы хорошо, не существует, зато существуют хорошие аллергологи.
Ротовую полость нужно проверить у стоматолога, чтобы вылечить кариес. В противном случае можно начать лечить аллергию и ничего не вылечить, потому что процессу будут мешать хронические заболевания носоглотки. Поэтому к диагностике мы подходим очень ответственно, и здесь я не обойдусь без клише: в каждом случае всё индивидуально. Волшебных таблеток, которые можно было бы выпить всем подряд и сразу стало бы хорошо, не существует, зато существуют хорошие аллергологи.
Предположим, что ЛОР и стоматолог заключили, что всё чисто. Это и хорошая, и плохая новость, так как теперь вам точно к аллергологу. На приёме врач подробно расспросит о характере симптомов, об устройстве быта: какой состав у подушки и одеяла (натуральные или искусственные ткани), есть ли домашние животные, на каком этаже живёте, сыро ли дома, есть ли подвал, многоквартирный или частный дом.
Если после такого блиц-опроса врач понимает, что пахнет жареным (точнее, пыльным), то начинаем планировать диагностику. Есть два основных метода:
- Кожные прик-тесты.

- Исследование специфических IgE (метод ImmunoCap).
Прик-тест (от английского prick — укол) — это кожный тест, который выполняется специальным инструментом, прик-ланцетом. Простыми словами, это такая иголка-царапка, которая делает насечки на передней поверхности предплечья глубиной не более чем 1-1,5 мм. Процесс безболезненный и бескровный. На получившиеся насечки врач капает специальный экстракт — аллерген, а также раствор гистамина (положительный контроль) и раствор натрия хлорида (отрицательный контроль). Пациент неподвижно сидит 20 минут и ждёт, а потом врач смотрит на реакцию кожи, измеряя линейкой появившуюся гиперемию (покраснение кожи) и папулу (волдырь).
Одновременное тестирование к нескольким аллергенам, для удобства врач чертит сетку и нумерует каждый.
Прик-тесты — это самый старый способ определения реакции организма на конкретный аллерген. Из плюсов: это быстро. Из минусов: ограничения по приёму антигистаминных препаратов, иногда случается дефицит экстрактов, есть небольшие ограничения по возрасту. Ключевой же минус метода в том, что это не очень удобно, ведь неподвижно высидеть в течение 20 минут — задача не из лёгких. Особенно если ты ребёнок.
Ключевой же минус метода в том, что это не очень удобно, ведь неподвижно высидеть в течение 20 минут — задача не из лёгких. Особенно если ты ребёнок.
Но главная беда с кожными тестами в том, что экстракты аллергена не умеют показывать реакцию на конкретный белок этого аллергена. По сути, врач получает минимум информации, и лечение приходится назначать практически вслепую только на основе своего опыта. Мне здесь очень нравится аналогия с салатом оливье: прик-тест может показать, что у вас аллергия на «оливье». Но на что именно — на горошек, на морковь, на картошку или на майонез, — такого прик-тест не расскажет. Пыль — это тоже своеобразный многокомпонентный «салат», и если в случае с оливье его можно просто перестать готовить, то от пыли мы, как уже говорили, не избавимся. Поэтому нам полезно знать, на какой именно из её компонентов у нас аллергия, чтобы спланировать мероприятия по лечению.
Для того чтобы получить максимально точный результат, мы отправляем пациента на анализ крови. В мире аллергодиагностики есть общепризнанный стандарт — молекулярная диагностика методом ImmunoCAP (аллергочип). На рынке есть и другие методы (к примеру, Rida, различные иммуноферментные анализы и так далее), но именно иммунокап является золотым стандартом.
В мире аллергодиагностики есть общепризнанный стандарт — молекулярная диагностика методом ImmunoCAP (аллергочип). На рынке есть и другие методы (к примеру, Rida, различные иммуноферментные анализы и так далее), но именно иммунокап является золотым стандартом.
Почему так? Дело в том, что в сыворотке нашей крови концентрация антител IgE (маркеры аллергических заболеваний) гораздо ниже, чем антител любых других классов. Значит, чтобы их обнаружить, нужен аллерготест с очень серьёзным уровнем чувствительности. На сегодняшний день такое умеет только ImmunoCAP: тест способен определить даже одну молекулу IgE. Даже в засохшей капле крови. Это лучший мировой показатель, поэтому звание «золотой стандарт» ImmunoCAP носит заслуженно.
Результаты такого анализа показывают, какие белки в аллергической реакции будут мажорными (главными), а какие — минорными (второстепенными). Именно мажорные белки указывают на развитие аллергии, и только они поддаются лечению аллерген-специфической терапией (АСИТ). И тут мы переходим к вариантам лечения.
И тут мы переходим к вариантам лечения.
Как будем лечить
Существует три основных метода лечения сенсибилизации к бытовой пыли:
- Элиминационные мероприятия (исключение контакта с аллергеном).
- Аллерген-специфическая иммунотерапия (АСИТ).
- Симптоматическая терапия: антигистаминные, гормоны, антилейкотриеновые.
Предположим, что к нам обратились родители ребёнка четырёх лет, и по результатам первичной диагностики мы подозреваем сенсибилизацию к пыли. Результаты прик-теста нам это подтверждают. В этом случае мы назначаем элиминационные мероприятия, что предполагает изолирование чада от контакта с пылью.
Элиминация аллергенов пыли
Во-первых, во время уборки рекомендуется выводить ребёнка на улицу. Размахивать веником = поднимать пыль в воздух, чего нам нужно избежать, поэтому используем специальные салфетки для уборки, воздухоочистительные приборы с фильтрами и пылесос с гиппоаллергенным фильтром. Аллергены в пыли настолько крошечные, что спокойно возвращаются обратно в воздух сквозь обычные пылесборные мешки, бумажные и тканевые фильтры в пылесосах. Чтобы аллергены не вырвались обратно, нужен хороший выходной фильтр — HEPA (High Efficiency Particulate Air). Есть классификация HEPA-фильтров: чем выше двузначное число в названии, тем больше частиц пыли он может удержать. Ещё аллергикам хорошо поможет пылесос с аквафильтром, в котором будут оседать мельчайшие частички пыли и аллергены в них.
Аллергены в пыли настолько крошечные, что спокойно возвращаются обратно в воздух сквозь обычные пылесборные мешки, бумажные и тканевые фильтры в пылесосах. Чтобы аллергены не вырвались обратно, нужен хороший выходной фильтр — HEPA (High Efficiency Particulate Air). Есть классификация HEPA-фильтров: чем выше двузначное число в названии, тем больше частиц пыли он может удержать. Ещё аллергикам хорошо поможет пылесос с аквафильтром, в котором будут оседать мельчайшие частички пыли и аллергены в них.
Схема устройства HEPA-фильтра.
Подушку и одеяло рекомендуется менять два раза в год. Клещам нравится жить в натуральных тканях: им там тепло, влажно, сытно и очень комфортно. По этой причине аллергикам не рекомендованы перьевые подушки, пуховые и ватные одеяла — только синтетические заменители. Также стоит приобрести гипоаллергенные наматрасники, наволочки, пододеяльники.
Клещи заселяют наши ковры и мягкие игрушки, поэтому их количество также нужно минимизировать и следить, чтобы они были сделаны из синтетических тканей.
В составе пыли, как мы помним, есть шерсть и частички эпидермиса домашних животных, поэтому контакт с питомцем также придётся ограничить. Чтобы исключить риск грибковой аллергии, лучше отказаться от комнатных растений и следить за уровнем влажности, не давая ему расти выше 50–60 %. Здесь у нас получается палка о двух концах, поскольку слишком сухой воздух — это не есть хорошо для нашей кожи и слизистой оболочки. Также есть результаты исследований, которые подтверждают, что приступы астмы, вызванные физическими усилиями, чаще случаются в сухом климате, чем во влажном.
Всё вышеописанное звучит логично и вполне закономерно, но, к сожалению, не является непосредственно лечением аллергии. Причина довольно проста: пыль всё равно никуда не денется. Давайте теперь продолжим историю с нашим пациентом: он уже подрос, ему исполнилось пять лет, и ЛОР диагностирует ему ринит. Ринит + аллергия на пыль — это бронхи в состоянии гиперреактивности, и при каком-либо раздражении дело может дойти до обструкции. Мы отправляем пациента на анализ крови методом Иммунокап и получаем подтверждение сенсибилизации к клещам домашней пыли.
Мы отправляем пациента на анализ крови методом Иммунокап и получаем подтверждение сенсибилизации к клещам домашней пыли.
Аллергическим реакциям вообще свойственно расти, как снежный ком, и у нашего пациента становится возможен риск развития бронхиальной астмы. На этом этапе мы рекомендуем проведение АСИТ, чтобы не допустить развития более тяжёлых симптомов аллергии.
Как работает аллерген-специфическая иммунотерапия (АСИТ)
Аллерген-специфическая иммунотерапия — это такая школа для иммунитета, которая заново учит его взаимодействовать с аллергеном: мы заменяем аллергический ответ иммунитета к конкретному аллергену на толерантный ответ. Такое «переучивание» происходит путём последовательного введения доз аллергена в наш организм, что в целом можно сравнить с процессом вакцинации. АСИТ работает таким образом, что с получением каждой новой дозы аллергена организм реагирует на него всё слабее и слабее.
АСИТ-терапия выполняется в виде подкожных инъекций и сублингвальным методом (подъязычно). Детям я не делаю парентеральную АСИТ: это как минимум негуманно, и есть клинические рекомендации, по которым АСИТ противопоказана до пяти лет. В результате контролируемого введения небольших доз аллергена в организм мы снижаем выработку IgE (класс антител, которые рулят аллергической реакцией) и стимулируем выработку IgG (класс антител, которые берут на себя удар и не запускают аллергическую реакцию при контакте с аллергеном в отличие от IgE).
Детям я не делаю парентеральную АСИТ: это как минимум негуманно, и есть клинические рекомендации, по которым АСИТ противопоказана до пяти лет. В результате контролируемого введения небольших доз аллергена в организм мы снижаем выработку IgE (класс антител, которые рулят аллергической реакцией) и стимулируем выработку IgG (класс антител, которые берут на себя удар и не запускают аллергическую реакцию при контакте с аллергеном в отличие от IgE).
Инъекционная АСИТ проводится в два этапа:
- Достижение максимальной терапевтической дозы.
- Этап поддерживающей терапии.
Как правило, первый этап длится три–шесть месяцев с введением аллергена в организм один-два раза в неделю. Второй же этап может длиться от трёх до пяти лет. Конечно, вы можете сказать, что у вас ещё куча других важных дел в жизни и можно просто закинуться антигистаминными. Тут нужно не забывать, что АСИТ — это единственный способ именно лечения аллергии, а не просто возможность временно заглушить симптомы.
АСИТ сублингвальным методом (то есть подъязычно) обычно длится около 12 месяцев. На отечественном рынке есть раствор клещей домашней пыли, а в 2022 году ожидаем появления аллергена в таблетках. То есть сенсибилизацию к пылевым клещам мы лечим подъязычно.
Об эффективности АСИТ наглядно говорят результаты метаанализов. Например, на картинке выше показано, как АСИТ предотвращает обострение симптомов астмы.
На каждые 100 пациентов, проходящих лечение аллерген-специфической иммунотерапией, приходится 30 человек, у которых приступ астмы благодаря АСИТ будет предотвращён, у 40 человек его бы больше и не случилось, и лишь у 30 приступы продолжатся.
Важный момент: в России нет препаратов АСИТ с аллергенами грибков и шерсти домашних животных. То есть если на клещей аллергии нет, а на грибки и шерсть животных есть, то АСИТ не показана по причине отсутствия препаратов.
Антигистаминные препараты
Третий способ борьбы с аллергией — принятие антигистаминных препаратов. Их называют препаратами симптоматической терапии, что буквально означает снятие симптомов аллергии. Гистамин — это такой вездесущий парень, пронизывающий все наши тучные клетки и являющийся итогом аллергической реакции, когда происходит выброс медиатора аллергического воспаления. Реакции, которые вызывает такой медиатор, — отёки, покраснение и зуд.
Их называют препаратами симптоматической терапии, что буквально означает снятие симптомов аллергии. Гистамин — это такой вездесущий парень, пронизывающий все наши тучные клетки и являющийся итогом аллергической реакции, когда происходит выброс медиатора аллергического воспаления. Реакции, которые вызывает такой медиатор, — отёки, покраснение и зуд.
Препараты первого поколения проникают через гематоэнцефалические барьеры (это такой фильтр между нашей кровеносной системой и центральной нервной системой, через которую в мозг поступают различные питательные, биоактивные и частично лекарственные вещества), что становится причиной разных неприятных эффектов (например, сонливость, угнетение сознания, влияние на способность управлять транспортным средством). Эти препараты не избирательны и, проникая в наш мозг, блокируют все рецепторы подряд. Пример антигистаминных препаратов первого поколения: Супрастин, Вигил, Диазолин. Сегодня они назначаются редко и применяются ограниченно.
Препараты второго поколения — результат прогрессивного развития медицины, они уже не имеют такого ярко выраженного седативного эффекта. Эти препараты научились избирательно блокировать только те гистаминовые рецепторы, которые нужно заблокировать. Ко второму поколению относятся, например, Лоратадин, Цетиризин, Эбастин, Биластин.
Эти препараты научились избирательно блокировать только те гистаминовые рецепторы, которые нужно заблокировать. Ко второму поколению относятся, например, Лоратадин, Цетиризин, Эбастин, Биластин.
Цетиризин был пионером среди антигистаминных второго поколения. Он представляет собой смесь из двух видов изомеров, которая блокирует гистаминовые рецепторы. С течением времени было обнаружено, что один из двух изомеров (правый), в общем-то, бесполезен, научились выделять только очищенный левый и дали ему логичное название — Левоцетиризин. В мире бессмысленного и беспощадного маркетинга существует третье поколение антигистаминных, к которым чаще всего относят Левоцетиризин, но официального обоснования этот рекламный трюк не имеет. Левоцетиризин также относится ко второму поколению.
Назначать антигистаминные второго поколения мы будем в трёх случаях аллергической реакции (когда нужно заблокировать h2-рецепторы, отвечающие за аллергический ответ):
- Аллергический конъюнктивит.

- Аллергический ринит.
- Крапивница.
Существуют и другие виды рецепторов и их гистаминовых блокаторов: h3-блокаторы (антигистаминные, которыми можно лечить заболевания желудка), h4-блокаторы (для терапии неврологических заболеваний).
Наверное, многие из вас когда-то пили антигистаминные. Это как такая палочка-выручалочка: началась крапивница, покрылись волдырями, всё чешется и вообще как-то страшно. А тут выпил таблетку, немножко подождал — и всё прошло. Красота же! Почему бы не закупиться впрок, не разложить таблетки по всем карманам и не прожить так всю свою долгую и счастливую жизнь?
Ответ на этот вопрос я уже на самом деле давала: аллергическим реакциям свойственно усугубляться и расти, как снежный ком.
Если вы заболеете ОРВИ, то сочетание насморка, кашля и прочих респираторных чудес с аллергией может превратиться в триггер для астмы, и тогда случится приступ. Антигистаминные всё же могут иногда не оказаться в кармане. Медицина не зря придумала молекулярные тесты крови, которые помогут узнать, сможет ли АСИТ облегчить ваши страдания. Это более надёжный способ лечить аллергию (именно лечить, а не глушить симптомы).
Медицина не зря придумала молекулярные тесты крови, которые помогут узнать, сможет ли АСИТ облегчить ваши страдания. Это более надёжный способ лечить аллергию (именно лечить, а не глушить симптомы).
Помимо профилактики астмы, мы также не допускаем расширения спектра аллергенов.
Итого
Сенсибилизация к пыли — штука не очень приятная, но мы научились с ней справляться. Если вы заподозрили у себя аллергию на пыль, то найдите хорошего аллерголога, который комплексно проведёт диагностику и при необходимости отправит вас на приём к другим врачам (ЛОР, стоматолог).
Лучшим методом диагностики будет ImmunoCAP. Если мы понимаем, что у вас аллергия только на грибок и шерсть животных, то рассказываем вам, как максимально оградить себя от этих аллергенов. Если находим сенсибилизацию к клещам домашней пыли, то назначаем АСИТ.
Не стоит медлить, если есть аллергический ринит и чувствительность к полевому клещу: это может привести к астме.
Если доберётесь до клиники, где я принимаю — «Наше время», — то говорите, что вы с Хабра: будет скидка 5 % на услуги (но не на препараты АСИТ).
Особенности бронхиальной астмы. Сочетанная сенсибилизация
Сочетанная сенсибилизация — это результат поливалентной сенсибилизации к 3 — 4 группам аллергенов.
Сочетанная аллергия создает трудности как в процессе диагностики заболевания — определения спектра аллергенов, так и в правильном выборе тактики лечения и последовательности лечения аллергенами при проведении специфической иммунотерапии.
Проявления сочетанной аллергии могут протекать по замедленному, немедленному, а также смешанному типам аллергических реакций и включать сенсибилизацию к разнородным аллергенам.
Сочетанная сенсибилизация пыльцевой этиологии отмечается при широко распространенных заболеваниях: атопическая бронхиальная астма, поллинозы, аллергический ринит, пищевая и лекарственная аллергия.
Значительный рост числа больных с одновременной сочетанной повышенной чувствительностью к различным аллергенам немикробного происхождения (бытовые, эпидермальные, пыльцевые и пищевые), вызывающим в организме формирование повышенной чувствительности немедленного типа с длительными периодами обострения и тяжелым течением аллергического процесса, составляют проблему разработки методов коррекции этих состояний. Проблема полисенсибилизации к пыльцевым и пищевым аллергенам подробно представлена в исследованиях С. X. Хутуевой.
При аллергии к пыльце растений встречается аллергия к фруктам и овощам. У больных с повышенной чувствительностью к пыльце березы в качестве пищевых аллергенов выступают яблоки, вишня, персики, абрикосы, груши, морковь, сельдерей. В наших исследованиях описывается острая аллергическая реакция в виде анафилактического шока, развившегося при употреблении виноградного сока у больного с сенсибилизацией к пыльце сложноцветных и к пыльце амброзии.
Несмотря на отдельные исследования, проведенные по изучению сочетанной сенсибилизации к неинфекционным аллергенам, в настоящее время остаются неизученными особенности клинического течения бронхиальной астмы с сочетанной аллергией в зависимости от аллергенного спектра. Не разработаны вопросы взаимосвязи клинических и иммунологических диагностических критериев.
Под нашим наблюдением находилось 213 больных с сочетанной сенсибилизацией к 3 и 4 различным группам неинфекционных аллергенов. Из них 50,2% больных имели сочетанную аллергию к бытовым эпидермальным и пищевым аллергенам; у 25,3% была обнаружена сенсибилизация к бытовым, эпидермальным и пыльцевым аллергенам, а у 24,5% — к 4 группам аллергенов (бытовым, эпидермальным, пищевым и пыльцевым) (табл. 13).
Сочетанная сенсибилизация к бытовым, эпидермальным и пыльцевым аллергенам определена у 25% больных с бронхиальной астмой.
Особенности клинического течения бронхиальной астмы зависели от аллергенного спектра и клинических проявлений пыльцевой сенсибилизации.
При сочетанной бытовой и эпидермальной аллергии с сопутствующей сенсибилизацией к пыльце луговых трав, как правило, астма имела доброкачественное течение, так как пыльцевая аллергия сопровождалась только риноконъюнктивальным синдромом.
При сочетании бытовой и эпидермальной аллергии с сенсибилизацией к пыльце сорных трав, а именно к пыльце амброзии, астма приобретала рецидивирующее злокачественное течение, так как у большинства больных аллергия к пыльце амброзии сопровождалась пыльцевой астмой.
Если бытовая астма сочеталась с аллергией к пыльце луговых и сорных трав, то в период цветения луговых трав отмечался риноконъюнктивный синдром, а в период цветения сорных трав присоединялись тяжелые приступы удушья из-за аллергии к амброзии.
Пыльцевая сенсибилизация в большинстве случаев сопровождалась пыльцевой астмой: в период цветения амброзии у больных приступы удушья имели тяжелое течение, с трудом купировались из-за высокой концентрации амброзии в воздухе. Приступы удушья продолжались и зимой за счет имевшейся бытовой аллергии, но протекали легче и не сопровождались выраженным риноконъюнктивальным синдромом. У больных пыльцевая астма соответствовала периоду цветения луговых трав.
Приступы удушья продолжались и зимой за счет имевшейся бытовой аллергии, но протекали легче и не сопровождались выраженным риноконъюнктивальным синдромом. У больных пыльцевая астма соответствовала периоду цветения луговых трав.
Таблица 13. Особенности сочетанной сенсибилизации у больных с атопической бронхиальной астмой
Появление пыльцевой аллергии было подтверждено наличием положительного провокационного назального теста с аллергеном амброзии, положительными результатами в PACT и позитивным базофильным тестом. У тех больных, у которых летняя сезонность заболевания была обусловлена и сенсибилизацией к клещам, имели место различия в клинических проявлениях болезни. Если при аллергии к амброзии на фоне риноконъюнктивального синдрома развивались приступы астмы, то состояние больных резко ухудшалось днем, особенно в солнечную погоду.
При выраженном же клещевом компоненте превалировали приступы удушья дома ночью, в постели. В течение суток больные отмечали постоянное, временами усиливающееся, затрудненное дыхание. Состояние больных резко ухудшалось за счет воздействия «виновных» аллергенов: днем — высокая концентрация пыльцы амброзии в воздухе, ночью — тесный контакт с клещевым аллергеном. Наличие «клещевого» компонента при пыльцевой бронхиальной астме затрудняло дифференциальную диагностику атопических и инфекционно-зависимых форм болезни.
В течение суток больные отмечали постоянное, временами усиливающееся, затрудненное дыхание. Состояние больных резко ухудшалось за счет воздействия «виновных» аллергенов: днем — высокая концентрация пыльцы амброзии в воздухе, ночью — тесный контакт с клещевым аллергеном. Наличие «клещевого» компонента при пыльцевой бронхиальной астме затрудняло дифференциальную диагностику атопических и инфекционно-зависимых форм болезни.
Приводим пример тяжелого течения бронхиальной астмы с сочетанной бытовой, эпидермальной и пыльцевой сенсибилизацией.
Выписка из истории болезни №5812
Больной Б. А. направлен в аллергологическнй центр участковым врачом с диагнозом бронхиальная астма инфекционно-аллергической формы.
Жалобы больного на приступы удушья зимой и летом, насморки, заложенность носа, одышку, кашель с отделением мокроты слизистого характера.
Заболел впервые в 7-летнем возрасте, когда летом стали беспокоить насморки, чихание, зуд глаз, затем появились приступы удушья. До 15-летнего возраста болел только летом. Лечился у участкового врача амбулаторно и стационарно. С 23-летнего возраста болезнь стала беспокоить и зимой, заболевание приобрело круглогодичный характер. Зимой приступы Удушья беспокоили чаще дома ночью. В летнее время особенно тяжелым периодом считал август-сентябрь-октябрь. Необоснованные насморки, чихание, периодическая заложенность носа беспокоили и зимой, и летом.
До 15-летнего возраста болел только летом. Лечился у участкового врача амбулаторно и стационарно. С 23-летнего возраста болезнь стала беспокоить и зимой, заболевание приобрело круглогодичный характер. Зимой приступы Удушья беспокоили чаще дома ночью. В летнее время особенно тяжелым периодом считал август-сентябрь-октябрь. Необоснованные насморки, чихание, периодическая заложенность носа беспокоили и зимой, и летом.
Особенно состояние больного ухудшилось в 37 лет, когда частые астматические состояния явились основанием для назначения в участковой поликлинике преднизолона (30 мг в сутки по схеме). Приступы удушья протекали тяжело, с трудом купировались. Больной потерял трудоспособность, и в 40 лет больному определена 2 группа инвалидности. Несмотря на то, что поддерживающая доза гормональных препаратов была 4 таблетки преднизолона в сутки, приступы удушья продолжали беспокоить. Пользовался ингаляционными симпатомиметиками и теофедрином.
В детстве часто болел пневмониями, другие заболевания отрицает. Аллергологический анамнез не отягощен.
Аллергологический анамнез не отягощен.
В условиях аллергологического кабинета больному проведено общеклиническое и аллергологическое обследование.
На флюорограмме органов грудной клетки: усиление легочного рисунка в прикорневых зонах и нижних легочных полях, корни уплотнены, сердце без особенностей; на флюорограмме гайморовых пазух: пристеночное снижение пнев-матизации гайморовых пазух; заключение ЛОР-врача: хронический ринит с аллергическим компонентом; ЭКГ: 1) ритм синусовый правильный, 2) гипертрофия правого предсердия и правого желудочка, 3) диффузные изменения миокарда.
Аллергологическое обследование методом постановки кожно-аллергических скарификационных проб, а также базофиль-ного теста позволило выявить аллергию к клещевым, эпидермальным, пыльцевым аллергенам — луговым травам и пыльце амброзии. Определены специфические IgE-антитела к амброзии методом PACT (++). Атопический генез заболевания подтвержден определением общего иммуноглобулина Е, который равен 2000 МЕ/мл.
Окончательный диагноз: бронхиальная астма, атопическая форма, тяжелое течение. Гормонозависимый вариант. Аллергия к клещевым, эпидермальным аллергенам. Поллиноз: аллергический ринит, конъюнктивит, сенсибилизация к пыльце амброзии. ДН II ст., хроническое легочное сердце в стадии компенсации.
Таким образом, трактовка диагноза (инфекционно-аллергическая — атопическая форма бронхиальной астмы) у данного пациента, отсутствие своевременной аллерген-специфической иммунотерапии привели к тяжелому течению бронхиальной астмы, инвалидизации этого больного.
Сочетанная сенсибилизация к бытовым, эпидермальным, пищевым аллергенам определена у 50,2% (из 213) больных с бронхиальной астмой. У 23,4% из них клинические проявления пищевой аллергии были только в раннем детстве, как только стихала пищевая аллергия, течение бронхиальной астмы у них приобретало доброкачественный характер. У 75,7 ± 4,12% больных проявления пищевой аллергии сохранялись многие годы, они четко знали «свои» аллергены.
Больные в большинстве своем указывали на аллергию к яйцу, рыбе, молоку, меду, шоколаду, реже — к цитрусовым и клубнике. Отмечались кожные проявления — крапивница, отек Квинке, респираторный рино-трахеобронхиальный синдром (заложенность носа, кашель, свистящее дыхание). У некоторых больных пища оказывала астмогенное действие.
При пищевой аллергии на первом месте по аллергенности стояли яйца, мед, клубника, цитрусовые. Аллергические реакции на продукты протекали по немедленному типу, поэтому больные четко определяли значение пищевой аллергии в возникшем приступе астмы. Из них у большинства (62,0 ± 9,1%) имела место поливалентная сенсибилизация к пищевым продуктам, проявляющаяся в виде приступов бронхиальной астмы.
Сочетание «пищевой» и «бытовой» астмы формировало рецидивирующее течение, причем предупредить этот рецидив обычно не всегда удавалось, так как круг пищевых аллергенов с каждым годом расширялся, особенно в группе больных, не проходивших аллерген-специфическую иммунотерапию.
Высокие показатели IgE-антител выявлены у больных с имеющимися кожными проявлениями аллергии (718,7 МЕ/мл). Уровень общего IgE у больных с респираторными проявлениями пищевой аллергии был ниже (377,1 ME/мл). При астмогенном действии «аллергенной» пищи отмечены частые приступы удушья, формируя этим рецидивирующее и более тяжелое клиническое течение бронхиальной астмы.
Рецидивирующее течение бронхиальной астмы при сочетании бытовой, эпидермальной и пищевой аллергии у 54,2% больных поддерживалось также наличием выраженной сенсибилизации к клещу.
Выписка из истории болезни №5144
Больная Д. Ф. обратилась в аллергологический кабинет с жалобами на приступы удушья, свистящее дыхание, сухой кашель, чаще ночью. Выявлена сенсибилизация к клещевому и эпидермальному аллергенам.
Диагноз: атопическая бронхиальная астма. В анамнезе: пищевой аллергией страдает с 3 лет. После употребления шоколада, меда, цитрусовых была крапивница, а после яблок, помидоров, дыни, фиников возникли приступы удушья.
В 1985 году летом у больной после употребления вишни развился приступ удушья. Утром она обратилась к аллергологу; в момент осмотра отмечен бронхоспазм, прослушивались сухие хрипы. Однако мать решила убедиться в этом еще раз и вновь дала ей вишню в чае (дочь об этом не знала), тут же развилась немедленная аллергическая реакция в виде гиперемии лица, зуда и удушья. Атопический генез бронхиальной астмы, помимо резко положительных кожных проб с аллергеном домашней пыли, пера подушки, вишни, подтвержден также высоким уровнем общего иммуноглобулина Е (800 МЕ/мл).
Специфические IgЕ-антитела к вишне определены методом постановки прямого базофильного теста. Реакция была резко положительной — 30% (+++).
Все вышеизложенное позволяет утверждать наличие у ребенка помимо бытовой, эпидермальной аллергии, также аллергию и к пищевым продуктам с проявлениями крапивницы и пищевой астмы.
Следовательно, клинические проявления пищевой аллергии оказывали воздействие на клиническое течение бронхиальной астмы. При наличии этих проявлений бронхиальная астма имела рецидивирующее течение.
При наличии этих проявлений бронхиальная астма имела рецидивирующее течение.
Анализ причин, обусловивших тяжесть течения бронхиальной астмы при сочетании бытовой, эпидермальной и пищевой аллергии, показал важное значение при наличии сочетанной сенсибилизации провокационного влияния на частоту обострений употребление аллергенных продуктов.
Особый интерес представляла группа больных, имевшая сочетанную сенсибилизацию к 4 группам неинфекционных аллергенов — бытовым, эпидермальным, пищевым и пыльцевым. Она выявлена у 24,5% больных. Длительность наблюдения большинства больных составляла от 15 до 30 лет. Сочетанная аллергия формировалась в сроки от 3 до 18 лет.
Поливалентная сенсибилизация не всегда своевременно диагностировалась. При позднем присоединении пыльцевой аллергии чаще на фоне уже имеющейся бытовой или пищевой сенсибилизации кожно-аллергические пробы с пыльцевыми аллергенами на раннем этапе были отрицательными. Кожная чувствительность у этих больных появлялась значительно позже клинических проявлений.
Так, из 7 больных у 2 кожно-аллергические пробы стали положительными через 4 года, а у 5 — через 6-10 лет, что также приводило к поздней диагностике пыльцевой аллергии. В этих случаях только использование дополнительных методов диагностики, таких как PACT, базофильный тест Шелли и провокационные эндоназальные тесты, позволили подтвердить наличие истинной сенсибилизации.
Диагностика пищевой аллергии у больных с поливалентной сенсибилизацией встречала дополнительные трудности, так как хорошо известно, что диагностическая ценность кожных проб при пищевой аллергии невелика. Поэтому данные аллергологического анамнеза неоднократно проверялись составлением пищевых дневников, проведением элиминационных тестов. Больного обучали методам ведения пищевого дневника и составлению элиминационных диет и с последующим провокационным тестом — употреблением аллергенных продуктов.
Данные анамнеза о наличии пищевой аллергии в последующем проверялись и подтверждались результатами аллергологического обследования. Для подтверждения атопии у больных в этой группе определялся общий IgE, уровень которого колебался от 211 до 2400 МЕ/мл, средний показатель составил 718,6 ± 45,2 МЕ/мл.
Для подтверждения атопии у больных в этой группе определялся общий IgE, уровень которого колебался от 211 до 2400 МЕ/мл, средний показатель составил 718,6 ± 45,2 МЕ/мл.
Для примера приводим клиническое наблюдение больной с сочетанной сенсибилизацией.
Выписка из история болезни №453
Больная П. Н. обратилась к аллергологу с жалобами на приступы удушья в течение всего года, чаще дома, ночью, заложенность носа, чихание, зуд глаз, их гиперемию и зимой, и летом. Заболела впервые в 1973 году, в июне появился насморк, чихание, повышение температуры, а в августе — первый приступ удушья. В сентябре еще продолжал беспокоить насморк, чихание, зуд глаз. Зимой насморк продолжал беспокоить, приступы удушья имели место, но протекали легче. В июле 1974 года вновь риноконъюнктивальный синдром, в августе-сентябре — тяжелые приступы удушья, и так ежегодно клинические проявления довольно стабильно беспокоили больную. В последующем частые простудные заболевания, холецистит.
Аллергологический анамнез: у отца аллергический ринит, у дедушки по линии матери — крапивница, у родной старшей сестры — отек Квинке, поллиноз. У самой больной с детства аллергический диатез, пищевая аллергия, удушье после употребления куриного бульона, мяса курицы. Больная четко отмечает элиминационный характер бронхиальной астмы, так как живя в Ленинграде у сестры чувствовала себя хорошо, приступов удушья не было.
При постановке кожно-аллергических проб с бытовыми, эпидермальными и пыльцевыми аллергенами, реакции были резко положительные: с аллергеном домашней пыли +++, пера подушки +++, шерсти овцы +++, пробы пыльцевыми аллергенами были положительные. Девочке проводили ежегодно по одному курсу специфической иммунотерапии бытовыми и эпидермальными аллергенами, после чего в зимнее время приступы удушья прекратились, но летняя сезонность в заболевании сохранялась, т. е. в июне, июле, августе, сентябре беспокоил выраженный риноконъюнктивальный синдром и астма.
Дополнительно больной проведено специфическое лечение пыльцевыми аллергенами, и впервые в 1985 г. в летнее время у девочки не было приступов удушья, лишь беспокоили незначительные проявления риноконъюнктивального синдрома. СИТ проводилась на фоне элиминационной диеты. Бронхиальная астма в этом случае расценена как атопическая с сочетанной аллергией: пищевой, бытовой, эпидермальной. Только упорная аллерген-специфическая иммунотерапия в сочетании с элиминационной диетой позволила добиться хорошего терапевтического эффекта.
Таким образом, с первого дня обращения в аллергологический кабинет имела место полиаллергия — пищевая, пыльцевая, бытовая и эпидермальная с сохранившейся пищевой аллергией по настоящее время.
Клинические проявления пищевой аллергии у больных в этой группе оказывали влияние на течение бронхиальной астмы. Если пищевая аллергия имелась только в прошлом, то по мере угасания пищевой аллергии астма приобретала доброкачественное течение. Пищевая аллергия с кожными проявлениями мало влияла на течение бронхиальной астмы.
Пищевая аллергия с кожными проявлениями мало влияла на течение бронхиальной астмы.
Респираторные проявления пищевой аллергии способствовали изменению характера астмы, учащались приступы удушья, беспокоил постоянный аллергический ринит. У 30,0 ± 6,3% обследованных больных пища оказывала прямое астмогенное действие, и бронхиальная астма принимала рецидивирующий характер, крут пищевых аллергенов расширялся, и трудно было предугадать, какой из них спровоцирует приступ удушья.
При кожных проявлениях пищевой аллергии превалировала моно- и бивалентная аллергия (68,2%), при респираторных проявлениях — поливалентная сенсибилизация, 60% больных указывали на 3 — 8 причинно-значимых пищевых аллергенов. Они четко знали «свои» пищевые аллергены и старались выдерживать элиминационную диету, так как при малейших погрешностях диеты начинались проявления пищевой аллергии.
Пыльцевая сенсибилизация сопровождалась пыльцевой астмой у 57,7 ± 9,0% больных, у остальных 42,3 ± 6,8% больных имели место проявления ринита, конъюнктивита, симптомы пыльцевой интоксикации (головная боль, плохой сон, разбитость, слабость, ознобы).
Нами рассмотрена пищевая аллергия и ее взаимосвязь с различными формами сопутствующей сенсибилизации.
При наличии аллергии к луговым и сорным травам больные чаще указывали на аллергию к яйцу, рыбе, арбузам, а при наличии аллергии к пыльце деревьев в сочетании с аллергией к травам имелись указания на аллергию к косточковым фруктам, из них 9 больных имели аллергию к фруктам (яблокам, персикам, вишне, орехам, гранатам).
Наличие пищевой аллергии к косточковым фруктам у больных с аллергией к пыльце деревьев (ольхи, орешника, березы, дуба, вяза и др.) объясняется структурной связью между аллергенами пыльцы березы и пищевыми продуктами. При аллергии к пыльце растений довольно часто встречается аллергия к фруктам и овощам. Наиболее часто в качестве пищевых аллергенов выступают яблоки, вишня, персики, абрикосы, груши, морковь, сельдерей. Нами описана острая аллергическая реакция, развившаяся при употреблении меда у больного с сенсибилизацией к пыльце амброзии и анафилактический шок, развившийся при приеме стакана виноградного сока.
При наличии аллергии к пыльце деревьев, луговых и сорных трав, бытовым и эпидермальным аллергенам заболевание имело непрерывно рецидивирующее течение. Приступы удушья зимой беспокоили за счет сенсибилизации к бытовым эпидермальным аллергенам, в апреле-мае присоединялась аллергия к пыльце деревьев, в июне-июле аллергия к пыльце луговых трав, а в августе-сентябре за счет аллергии к амброзии. Именно эта группа больных была чрезвычайно сложной как в диагностическом, так и в лечебном плане.
Одна форма сенсибилизации присоединялась к другой, и бронхиальная астма приобретала тяжелое течение, к тому же у них у всех имелась поливалентня сенсибилизация с указанием от 3 — 8 аллергенных пищевых продуктов, а в спектр пыльцевых аллергенов включался аллерген амброзии. У 61,4% больных, помимо пыльцевой аллергии и пищевой аллергии, бытовая и эпидермальная аллергия сопровождалась выраженной сенсибилизацией к клещу.
Следовательно, тяжелое течение астмы зависело не только от аллергенного спектра, но и от клинических проявлений сопутствующих форм сенсибилизации. Сочетание у больного амброзийной, клещевой и пищевой астмы формировало тяжелое непрерывно рецидивирующее течение.
Сочетание у больного амброзийной, клещевой и пищевой астмы формировало тяжелое непрерывно рецидивирующее течение.
Следует отметить, что в этой группе длительность заболевания астмой у 95% составляла от 3 — 18 лет, и только у 5% больных длительность астмы была до 5 лет.
Приводим выписку из истории болезни больной бронхиальной астмой с полиаллергией к 4 группам аллергенов.
Выписка из истории болезни №445
Больная Л. Н. обратилась к аллергологу в 6-летнем возрасте с жалобами на приступы удушья экспираторного характера больше дома, ночью (дом частный, одноэтажный, темный), кашель с отделением слизистой мокроты, необоснованные насморки. Заболела впервые после перенесенной пневмонии. В последующем приступы удушья участились. Лечилась амбулаторно и стационарно. Аллергологический анамнез: у матери пищевая аллергия. В прошлом у самой больной аллергический диатез с двух месяцев, затем сыпь по телу при употреблении цитрусовых, шоколада, яиц, приступ удушья — после употребления мяса утки и рыбы.
Состояние больной стало резко ухудшаться в период с августа по сентябрь и даже октябрь, и проявлялось это риноконъюнктивальным синдромом в сочетании с приступами удушья. Больную обследовали в аллергологическом кабинете, выявили сочетанную бытовую, эпидермальную и пыльцевую аллергию. В период цветения амброзии (август-сентябрь) больная выезжала в Приэльбрусье, где чувствовала себя хорошо и возвращалась в г. Нальчик, когда амброзия уже отцветала.
Таким образом, бронхиальная астма началась в детском возрасте, полиаллергия формировалась поэтапно следующим образом: пищевая аллергия, бытовая, эпидермальная, пыльцевая аллергия к сорным травам.
Аллергологическое обследование подтвердило атопический характер заболевания, общий IgE — 500 МЕ/мл, кожно-аллергические пробы выявили аллергию к домашней пыли (++++), перу подушек (+++), шерсти овцы (++), к пыльце сорняков — амброзии ++++, полыни +++, лебеде ++, с пищевыми аллергенами — резко положительные реакции с аллергеном молока +++, яйца ++, утки ++. Специфический IgE, определенный методом PACT, подтвердил аллергию к пищевым аллергенам — молоку ++, яйцам ++, амброзии ++. Следовательно, у данной больной клинически и при специфическом аллергологическом обследовании подтверждена аллергия к 4 группам неинфекционных аллергенов.
Специфический IgE, определенный методом PACT, подтвердил аллергию к пищевым аллергенам — молоку ++, яйцам ++, амброзии ++. Следовательно, у данной больной клинически и при специфическом аллергологическом обследовании подтверждена аллергия к 4 группам неинфекционных аллергенов.
Таким образом, при аллергии к 4 группам аллергенов — бытовым, эпидермальным, пищевым и пыльцевым астма часто приобретала тяжелое рецидивирующее течение, что затрудняло этиологическую диагностику.
Хутуева С.X., Федосеева В.Н.
Опубликовал Константин Моканов
Размер домохозяйства связан с аллергической сенсибилизацией
Ричард Гавел
Взгляд Джозефа Д. Эрнандеса, доктора медицинских наук.
Факт проверен Кристен Дауд
Источник/раскрытие информации
Источник:
Понсонби А.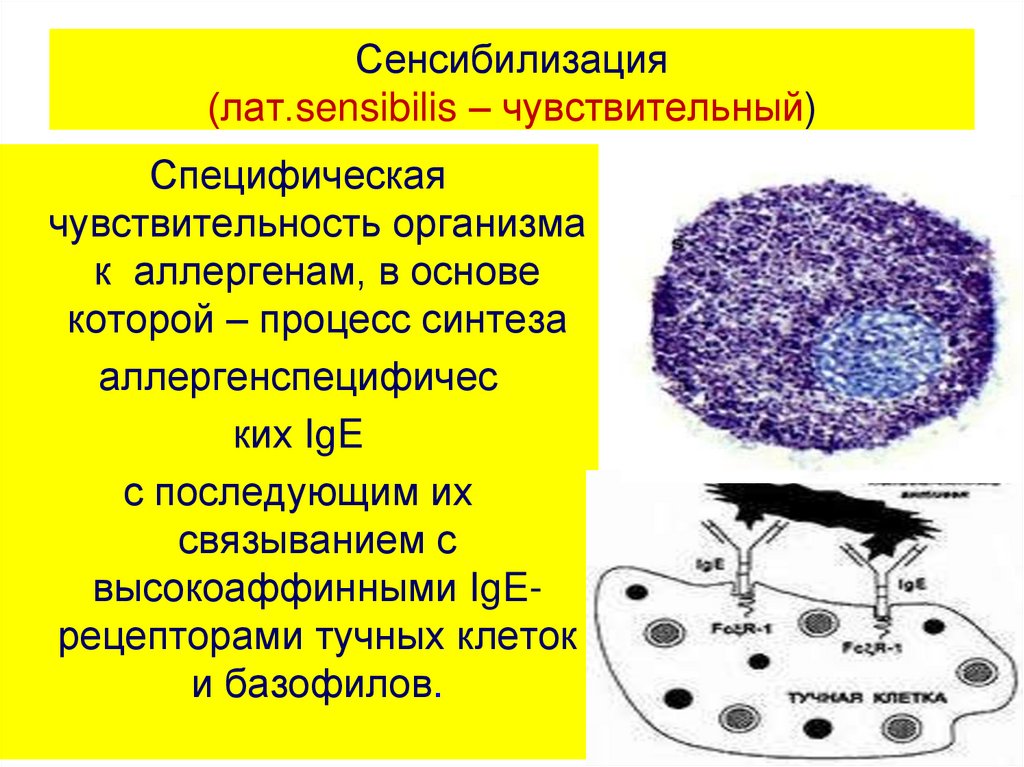 Л. и соавт. Педиатр Аллергия Иммунол . 2022; doi: 10.1111/pai.13810.
Л. и соавт. Педиатр Аллергия Иммунол . 2022; doi: 10.1111/pai.13810.
Раскрытие информации: Понсонби сообщает о получении стипендии от Национального совета по здравоохранению и медицинским исследованиям. Пожалуйста, ознакомьтесь с исследованием для всех соответствующих раскрытий финансовой информации других авторов.
Вы успешно добавили оповещения. Вы получите электронное письмо, когда будет опубликован новый контент.
Щелкните здесь, чтобы управлять оповещениями по электронной почте
Нам не удалось обработать ваш запрос. Пожалуйста, попробуйте позже. Если у вас по-прежнему возникает эта проблема, свяжитесь с нами по адресу [email protected].
Исследователи обнаружили связь между большими домохозяйствами и более высоким уровнем наивных регуляторных Т-клеток, что, в свою очередь, было связано с меньшей аллергической сенсибилизацией и заболеванием в возрасте 12 месяцев, согласно исследованию.
Также была выявлена связь между множественными пренатальными и постнатальными микробными факторами и развитием наивных Т-регуляторных (nTreg) и активированных Т-регуляторных (aTreg) клеток, как пишут исследователи в исследовании, опубликованном в журнале Pediatric Allergy and Immunology 9.0017 .
Источник: Adobe StockПод руководством Энн-Луизы Понсонби, BMedSci, MBBS, PhD, FAFPHM, FRACP, профессора Института неврологии и психического здоровья Флори в Парквилле, Австралия, исследователи заявили, что FoxP3-позитивные Treg-клетки помогают поддерживать иммунную толерантность к пищевым продуктам. и другие аллергены окружающей среды.
В ответ на антигенную иммуностимуляцию, продолжили исследователи, клетки nTreg в кровотоке могут стать клетками aTreg. Ранее исследователи сообщали, что дефицит клеток nTreg при рождении предсказывает пищевую аллергию в возрасте 1 года.
Исследователи изучили данные, в том числе 19 пренатальных микробных факторов окружающей среды, из исследования Barwon Infant Study 1074 младенцев, рожденных женщинами, набранными в период с июня 2010 г. по июнь 2013 г. те, у кого были большие семьи из трех или более жителей и одного или более братьев и сестер, имели более высокие пропорции nTreg в пуповинной крови ( P < 0,0001).
по июнь 2013 г. те, у кого были большие семьи из трех или более жителей и одного или более братьев и сестер, имели более высокие пропорции nTreg в пуповинной крови ( P < 0,0001).
Исследователи также обнаружили связь между более высокими уровнями nTreg и рядом микробных факторов окружающей среды в возрасте 6 и 12 месяцев (n = 19).1). Например, исключительное или смешанное грудное вскармливание по сравнению с отсутствием грудного вскармливания имело более сильную связь с более высокими уровнями nTreg в возрасте 6 месяцев.
Исследователи также обнаружили небольшую связь между микробными факторами окружающей среды и долей аТрег при рождении; тем не менее, они обнаружили связь между большим размером домохозяйства и более высоким уровнем аТрег в возрасте 6 месяцев.
В возрасте 12 месяцев исследователи обнаружили связь между более высокими уровнями aTreg и владением собакой, а также более высокими профессиональными социальными контактами матери и отца, включая доказательства реакции на дозу.
В течение первого постнатального года более высокие доли nTreg ( P < 0,001) и aTreg ( P = 0,007) были обнаружены среди младенцев из более крупных домохозяйств, при этом более высокие доли nTreg были обнаружены среди младенцев с собакой ( P = 0,01).
Кроме того, у детей, находящихся на грудном вскармливании, были более высокие продольные пропорции nTreg и aTreg. Те, кто посещал формальный уход за детьми, имели более высокие продольные доли nTreg ( P = 0,02), но не пропорции aTreg в первый постнатальный год.
Основываясь на анализе рабочих характеристик приемника, исследователи обнаружили, что у младенцев с 3 % или более nTreg при рождении значительно реже возникают аллергические реакции, включая пищевую аллергию (скорректированное ОШ = 0,21; 95 % ДИ, 0,09–0,5) и атопический дерматит. экзема (aOR = 0,26; 95% ДИ, 0,1-0,64).
Также исследователи обнаружили сильную связь между полисенсибилизацией в возрасте 1 года и любым аллергическим заболеванием, включая пищевую аллергию, атопическую экзему и/или атопическую астму, в возрасте 4 лет (aOR = 9). 0,26; 95% ДИ, 2,46-34,85).
0,26; 95% ДИ, 2,46-34,85).
Снижение риска аллергической полисенсибилизации, пищевой аллергии, атопической экземы и атопического хрипа к возрасту 1 года было связано с более высоким содержанием nTreg в пуповинной крови. Кроме того, больший размер домохозяйства имел наиболее последовательную связь среди оцениваемых микробных факторов с увеличением доли нТрег в пуповинной крови при рождении и с более высокими долями нТрег и аТрег в течение первого постнатального года.
В целом, исследователи пришли к выводу, что существует связь между большим размером домохозяйства и более высокими пропорциями nTreg при рождении, а также более высокими пропорциями nTreg и aTreg в течение первого постнатального года.
Однако эти более высокие пропорции nTreg при рождении, а не в возрасте 6 или 12 месяцев, предсказывают аллергические исходы к возрасту 12 месяцев, указывая на то, что неадекватное пренатальное иммунное праймирование играет важную роль в развитии аллергических заболеваний.
Отметив несколько признаков, указывающих на возможную причинно-следственную связь, исследователи призвали к дополнительным исследованиям, чтобы оценить роль иммунного прайминга предыдущих беременностей у матери, а также влияние продолжительности родов.
Эпигенетические исследования также должны быть включены в исследования пренатального программирования Treg-клеток, наряду с влиянием микробиомов кишечника матери и ребенка на иммунный профиль ребенка, добавили исследователи.
Жилая зелень, астма и функция легких у детей с высоким риском аллергической сенсибилизации: проспективное когортное исследование
- Данные и инструменты
- Публикации
- Мультимедиа
| Авторов: | Ким Хартли, Патрик Х. Райан, Гордон Л. Гиллеспи, Джозеф Пераццо, Дж. Майкл Райт, Гленн Э. Райс, Джеффри Х. Донован, Ребекка Гернес, Гурджит К. Хурана Херши, Грейс ЛеМастерс, Коул Брокамп Райан, Гордон Л. Гиллеспи, Джозеф Пераццо, Дж. Майкл Райт, Гленн Э. Райс, Джеффри Х. Донован, Ребекка Гернес, Гурджит К. Хурана Херши, Грейс ЛеМастерс, Коул Брокамп |
| Год: | 2022 |
| Тип: | Научный журнал (JRNL) |
| Станция: | Тихоокеанская северо-западная исследовательская станция |
| DOI: | https://doi.org/10.1186/s12940-022-00864-w |
| Источник: | Гигиена окружающей среды. 21(1): 675-687. |
Аннотация
Справочная информация: Несмотря на то, что сообщалось о пользе зеленого цвета для здоровья, данные, относящиеся к респираторному здоровью детей, противоречивы.
Методы. Мы использовали предполагаемую возрастную когорту, за которой наблюдали от рождения до 7 лет ( n = 617). Окружающая жилая зелень была количественно оценена с помощью индекса нормализованной разности растительности (NDVI) на расстоянии 200, 400 и 800 м от геокодированных домашних адресов при рождении, в возрасте 7 лет и в детстве. Исходы респираторного здоровья оценивались в возрасте 7 лет, включая астму и функцию легких [процент прогнозируемого объема форсированного выдоха в первую секунду (%FEV 1 ), процент прогнозируемой форсированной жизненной емкости легких (%FVC) и процент прогнозируемого соотношения форсированного выдоха объема за первую секунду до форсированной жизненной емкости легких (%ОФВ 1 /ФВК)]. Мы оценили ассоциации, используя модели линейной и логистической регрессии, скорректированные с учетом лишений сообщества, доходов домохозяйств и загрязнения воздуха, связанного с дорожным движением. Мы проверили модификацию измерения эффекта в зависимости от атопического статуса.
Исходы респираторного здоровья оценивались в возрасте 7 лет, включая астму и функцию легких [процент прогнозируемого объема форсированного выдоха в первую секунду (%FEV 1 ), процент прогнозируемой форсированной жизненной емкости легких (%FVC) и процент прогнозируемого соотношения форсированного выдоха объема за первую секунду до форсированной жизненной емкости легких (%ОФВ 1 /ФВК)]. Мы оценили ассоциации, используя модели линейной и логистической регрессии, скорректированные с учетом лишений сообщества, доходов домохозяйств и загрязнения воздуха, связанного с дорожным движением. Мы проверили модификацию измерения эффекта в зависимости от атопического статуса.
Результаты. Мы отметили признаки положительного смешения, поскольку обратные ассоциации ослаблялись при корректировке многомерных моделей. Мы обнаружили доказательства модификации измерения эффекта NDVI и астмы в пределах 400 м в возрасте 7 лет в зависимости от атопического статуса (9).0144 p = 0,04), при этом дети, сенсибилизированные к общим аллергенам, с большей вероятностью заболевали астмой по мере увеличения воздействия зелени (OR = 1,3, 95% ДИ: 0,9, 2,0) по сравнению с детьми, не сенсибилизированными к общим аллергенам (OR = 0,8, 95). % ДИ: 0,5, 1,2). Мы обнаружили последовательно положительные ассоциации между NDVI и %FEV 1 и %FVC, которые также свидетельствовали о положительном искажении при корректировке. В скорректированных регрессионных моделях NDVI в возрасте 7 лет был связан с % FEV 1 (200 м: β = 2,1, 95% ДИ: 0,1, 3,3; 400 м: β = 1,6, 95% ДИ: 0,3, 2,9) и %ФЖЕЛ (200 м: β = 1,8, 95% ДИ: 0,7, 3,0; 400 м: β = 1,6, 95% ДИ: 0,3, 2,8; 800 m: β = 1,5, 95% ДИ: 0,1, 2,8). Скорректированные результаты для %FEV 1 /FVC были незначительными, за исключением воздействия при рождении в 400-метровом буфере (β = 0,81, 95% ДИ: 0,1, 1,5). Мы не обнаружили никаких доказательств того, что изменение показателя NDVI в зависимости от атопического статуса влияет на объективные показатели функции легких.
% ДИ: 0,5, 1,2). Мы обнаружили последовательно положительные ассоциации между NDVI и %FEV 1 и %FVC, которые также свидетельствовали о положительном искажении при корректировке. В скорректированных регрессионных моделях NDVI в возрасте 7 лет был связан с % FEV 1 (200 м: β = 2,1, 95% ДИ: 0,1, 3,3; 400 м: β = 1,6, 95% ДИ: 0,3, 2,9) и %ФЖЕЛ (200 м: β = 1,8, 95% ДИ: 0,7, 3,0; 400 м: β = 1,6, 95% ДИ: 0,3, 2,8; 800 m: β = 1,5, 95% ДИ: 0,1, 2,8). Скорректированные результаты для %FEV 1 /FVC были незначительными, за исключением воздействия при рождении в 400-метровом буфере (β = 0,81, 95% ДИ: 0,1, 1,5). Мы не обнаружили никаких доказательств того, что изменение показателя NDVI в зависимости от атопического статуса влияет на объективные показатели функции легких.
Вывод: Чувствительность к аллергенам может изменить влияние зелени на риск развития астмы у детей, но зелень, вероятно, полезна для одновременной функции легких независимо от аллергического статуса.
Ключевые слова
Детская, ребенок, зеленое пространство, зеленое пространство, респираторный, аллергия, Окружающая среда, атопия.
Цитата
Хартли, Ким; Райан, Патрик Х .; Гиллеспи, Гордон Л.; Пераццо, Джозеф; Райт, Дж. Майкл; Райс, Гленн Э.; Донован, Джеффри Х .; Гернес, Ребекка; Херши, Гурджит К. Хурана; ЛеМастерс, Грейс; Брокамп, Коул. 2022. Жилая зелень, астма и функция легких у детей с высоким риском аллергической сенсибилизации: проспективное когортное исследование. Состояние окружающей среды. 21(1): 675-687. https://doi.org/10.1186/s12940-022-00864-в.
Цитаты
☓
@article{Hartley_2022,
doi = {10.1186/s12940-022-00864-w},
url = {https://doi.org/10.1186%2Fs12940-022-00864-w} = 2, 2 0 864-w},
месяц = {май},
издатель = {Springer Science and Business Media {LLC}},
volume = {21},
number = {1},
author = {Ким Хартли, Патрик Х. Райан и Гордон Л. Гиллеспи и Джозеф Пераццо и Дж. Майкл Райт и Гленн Э. Райс и Джеффри Х. Донован и Ребекка Гернес и Гурджит К. Хурана Херши и Грейс ЛеМастерс и Коул Брокамп},
Райан и Гордон Л. Гиллеспи и Джозеф Пераццо и Дж. Майкл Райт и Гленн Э. Райс и Джеффри Х. Донован и Ребекка Гернес и Гурджит К. Хурана Херши и Грейс ЛеМастерс и Коул Брокамп},
title = {Зеленость жилых домов, астма и функция легких у детей с высоким риском аллергической сенсибилизации: проспективное когортное исследование},
journal = {Здоровье окружающей среды}
}
CopyDownload
TY — JOUR
DO — 10.1186/s12940-022-00864-w
UR — http://dx.doi.org/10.1186/s12940-022-00864-w
TI — Жилая зелень, астма и функция легких среди детей с высоким риском аллергической сенсибилизации: проспективное когортное исследование
T2 — Гигиена окружающей среды
AU — Хартли, Ким
AU — Райан, Патрик Х.
AU — Гиллеспи, Гордон Л.
AU — Пераццо, Джозеф
AU — Райт, Дж. Майкл
AU — Райс, Гленн Э.
AU — Донован, Джеффри Х.
AU — Гернес, Ребекка
AU — Hershey, Gurjit K. Khurana
Khurana
AU — LeMasters, Grace
AU — Brokamp, Cole
PY — 2022
DA — 12/05/2022
PB — Springer ООО «Наука энд Бизнес Медиа»
ИС — 1
ВЛ — 21
СН — 1476-069X
ER —
КопироватьЗагрузить
Влияние на изменение поведения посредством массовой сенсибилизации сообщества | Танзания
Четверг, 11 июня 2020 г.
коронавирус COVID-19
Автор: Агнесс Джон, старший специалист по связям с общественностью
Изменение поведения — это не однодневный процесс, а повседневный процесс, который требует коллективной ответственности. Организация World Vision в Танзании в сотрудничестве с Министерством здравоохранения, общественного развития, гендерного равенства, престарелых и детей (MoHCDEC) провела массовую разъяснительную работу среди населения в ответ на COVID-19.в районах Аруши, Дар-эс-Салама, Додомы и Кагеры.
В центре внимания массового просвещения были меры профилактики и контроля COVID-19, а также предотвращение гендерного насилия и насилия в отношении детей. Содействие проводилось сотрудником по развитию сообщества, сотрудником по социальному обеспечению, социальными работниками (CCW) и общественными работниками здравоохранения (CHW), которые прошли обучение по признакам и симптомам COVID-19, мерам профилактики и контроля, важности обращения за медицинской консультацией. , и ведение случаев в домашнем хозяйстве.
Это делается для обеспечения локализации, включая активное наблюдение, раннее выявление, изоляцию и ведение случаев, отслеживание контактов и предотвращение распространения.
«Регионы Аруша, Дар-эс-Салам, Додома и Кагера, находящиеся в зоне высокого риска, почти не затронутые коронавирусом и имеющие приоритет правительства, были проведены массовые мероприятия по информированию общественности в общей сложности в 126 деревнях. Обученные массовые просветители повышают осведомленность сообществ о коронавирусе, проводя посещения домохозяйств от двери к двери и в некоторых людных местах, таких как рынки, автобусные остановки и другие выявленные горячие точки. Наращивание потенциала варьируется от того, как COVID-19передается, его симптомы и меры профилактики, а также важность обращения за медицинской помощью при появлении симптомов», — сказала Джулиана Чарльз, менеджер по реагированию на COVID-19 World Vision в Танзании.
Наращивание потенциала варьируется от того, как COVID-19передается, его симптомы и меры профилактики, а также важность обращения за медицинской помощью при появлении симптомов», — сказала Джулиана Чарльз, менеджер по реагированию на COVID-19 World Vision в Танзании.
Вмешательство также было направлено на оценку уровня осведомленности о заболевании на уровне домохозяйства и сообщества в целом. Министерство здравоохранения, развития сообществ, гендерных вопросов, пожилых людей и детей (MoHCDGEC) возглавляет усилия по обеспечению надлежащего лечения случаев заболевания, а также обеспечению того, чтобы сообщества были хорошо осведомлены об этом заболевании.
«Несмотря на недавнее объявление о снижении передачи коронавируса, необходимо предупредить общественность и продолжать применять профилактические и контрольные меры, чтобы обеспечить полное искоренение болезни», — пояснил д-р Нафтали Нгонди, комиссар Танзании по вопросам здравоохранения. Социальное обеспечение. «Информационные сессии и разъяснительная работа на уровне домохозяйств в людных местах напомнили членам сообщества о необходимости соблюдать меры предосторожности и ограничить передачу инфекции».
Массовое информирование населения и посещение домохозяйств по COVID-19профилактические меры также предоставляют членам сообщества пространство для обсуждения и прояснения их сомнений и понимания, как отметила Гевальда Чарльз, жительница Дар-эс-Салама на улице Мбези Луис. «Многие семьи все еще беспокоились о том, что такое коронавирус, поскольку они в основном полагались на различные источники информации, такие как социальные сети и своих коллег по сообществу, которые полностью демонстрировали свое разочарование и вызывали беспокойство у сообщества. Эта сессия дала нам время, чтобы получить проработку, отличную от предыдущих вмешательств по созданию осознания».
Помимо наращивания потенциала в области борьбы с коронавирусом, необходимо было обучение по вопросам предотвращения гендерного насилия и насилия в отношении детей. Закрытие школ подвергает детей, девочек и мальчиков большему риску насилия и жестокого обращения. «Мы помогаем родителям и опекунам, защищая себя и семьи от заражения COVID-19, они также должны защищать детей от детских браков, ранней беременности, сексуального насилия, детского труда и телесных наказаний», — сказал Годфри Кисемба, представитель World Vision в Танзании. Координатор по гендерным вопросам, адвокации и кампаниям.
Координатор по гендерным вопросам, адвокации и кампаниям.
Поскольку мы боремся с COVID-19, защита детей находится на первом месте во всем, что мы делаем, поэтому мы привлекаем всех вокруг, чтобы обеспечить надежную защиту детей.
«В ходе этой массовой сенсибилизации сообщества мы узнали об ограниченном понимании COVID-19. Мы также обнаружили, что большинство детей оказались на улице в результате закрытия школ, поэтому мы настаивали на том, чтобы родители и лидеры следили за тем, чтобы каждый родитель держал своих детей дома и прекратил вовлекать их в бизнес. Деревенские исполнительные директора находятся рядом с деревней, поэтому мы даем им возможность быть на переднем крае, чтобы сообщество могло подражать их передовым методам». Люси Ньела, специалист по развитию сообщества, округ Саланга в Дар-эс-Саламе.
«Повышение осведомленности населения о мерах по профилактике и борьбе с коронавирусом было нашим приоритетом местного правительства, однако мы сталкиваемся с некоторыми проблемами, в том числе с тем, что матери отправляют своих детей на рынок, это решается, и продолжается наращивание потенциала».


